Чем отличается живая вакцина от неживой
Основная разница между живой и неживой вакцинами – то, что в основе первой содержатся живые микроорганизмы. Многие полагают, что поэтому она лучше и безопаснее, поскольку более естественна. На самом деле, это не совсем так. В различиях следует разобраться подробнее.
- Безопасность в применении. По этому поводу было проведено много исследований, в результате которых выявлено, что ни одно из средств не может спровоцировать аллергию. Уровень безопасности одинаковый. При этом живые вакцины всё же не применяют у пациентов с такими болезнями, как ВИЧ или онкология, чтобы не ослабить иммунитет ещё больше, ведь при введении живого микроба, пусть и инактивированного, есть вероятность развития настоящего заболевания.
- Достижение эффекта. Живая вакцина при однократном введении способна сформировать иммунитет на длительный срок. Неживая требует ревакцинации, хотя эффект тоже достаточно хорош.
- Воздействие. Действующие вещества живых препаратов начинают работу мгновенно, результат появляется сразу. Чтобы добиться эффекта от неживой вакцины, нужно завершить курс, включающий обычно два или три укола.
Существенных различий между живыми и неживыми вакцинами нет, поэтому, изучив инструкции к ним, пациент сам принимает решение о необходимости использования того или иного препарата.
Правда ли, что вакцины обладают свойством убивать иммунную защиту ребенка?
Прививка действительно приводит к временному ослабеванию защитных сил. Это объясняется тем, что антигенный материал провоцирует определенные изменения в организме.
В ходе такого процесса, иммунная система занята борьбой с искусственно введенным патогеном. В период выработки антител ребенок становится уязвимым к некоторым заболеваниям.
Но после того как иммунный ответ сформируется, состояние нормализуется, организм становится крепче. Последние исследования американских ученых показали, что прививка не разрушает защитный барьер малыша. Были изучены медицинские сведения 944 детей возрастом от 2 до 4 лет.
Одних малышей повергли воздействию 193-435 антигенов, другие не получали плановые вакцины. В итоге оказалось, что никакой разницы в подверженности инфекционным и неинфекционным заболеваниям, у непривитых и иммунизированных нет. Единственное, вакцинированные стали защищенными от тех болезней, от которых они прошли профилактику.
Основные способы иммунизации
Способы прививания зависят от метода введения профилактического раствора с антигенами человеку. В клинической практике применяют ряд этих методик. В зависимости от их особенностей определяют, каким способом будет происходить прививание иммунного ответа:
- внутримышечный метод предполагает необходимость произведения инъекции в мышцы бедра, дельты (яркий пример – прививка с анатоксинами АКДС);
- подкожные прививки ставят в подлопаточную или плечевую область (такой вариант прививки отличается повышенной результативностью, низкой аллергенностью, простотой использования);
- внутрикожные вакцинные инъекции проводятся живой вакциной (БЦЖ, чумы, туляремии, лихорадки Ку);
- ингаляционный метод используется при проведении экстренной помощи (таким путем вводятся вакцины против столбняка, гриппа, дифтерийной интоксикации, краснухи, туберкулеза);
- пероральный прием — один из самых удобных вариантов иммунизации, так как средства вводятся через рот в виде капель (прививка от бешенства, вакцина от полиомиелита).
Внутримышечные, подкожные, внутрикожные прививки являются самыми неприятными для пациентов, так как вводятся путем прокола кожных покровов, доставляя человеку боль. Для устранения неприятных ощущений сегодня рекомендуют вводить препараты в виде аэрозолей или через рот. Помимо безболезненности, данные способы профилактической иммунизации отличаются высокой стерильностью и небольшим количеством послепрививочных осложнений.
Что такое вакцина
Вакцина это прививочный материал, в состав которого входят ослабленные или убитые микроорганизмы, либо их компоненты или вырабатываемые ними токсины. Введение вещества осуществляется только в поликлинике или больнице врачом или манипуляционной сестрой.
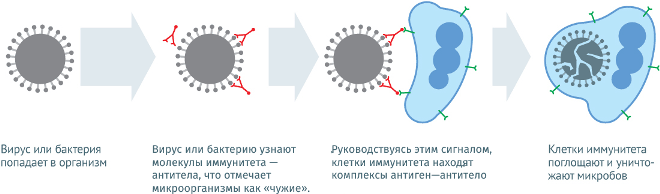
Принцип действия
Принцип действия основан на побуждении иммунной системы к выработке защитных антител к возбудителю и формированию специфического иммунитета. Компоненты прививки представляют собой своеобразный муляж, призванный выполнить тренировку организма. При этом входящие в состав вакцины микроорганизмы или их компоненты настолько слабы, что не способны вызвать заболевание. В конечном итоге иммунные клетки, ранее искусственно столкнувшиеся с вирусом, активно подавляют развитие болезни.
Важность применения вакцин
Иммунизация, выполненная посредством введения в организм вакцины, является единственным надёжным способом защиты от таких страшных заболеваний, как, например, оспа или полиомиелит.
Большинство заболеваний, от которых делаются прививки, во многих случаях оканчиваются для человека летальным исходом. В последнее время можно наблюдать широкий отказ от вакцинации, зачастую противники прививок обосновывают его отсутствием эпидемий той или иной болезни. Однако отсутствие эпидемий и является закономерным результатом своевременной вакцинации.
Предъявляемые требования
Ежегодно вакцины совершенствуются, разрабатываются всё более безопасные и надёжные препараты. Независимо от того, какие типы вакцин поставляются в медицинское учреждение, все они должны соответствовать следующим требованиям:
- быть иммуногенными, то есть вызывать защитную реакцию иммунитета;
- обладать низкой аллергенностью;
- не провоцировать онкогенность;
- иметь длительный срок хранения и простой порядок применения.
Высокие требования предъявляются также к технологии производства и штаммам, из которых изготовлена вакцина, – те должны быть генетически стабильны.
Живая вакцина
Живая вакцина – это незаменимый препарат для профилактики множества инфекционных заболеваний, который встречается только в корпускулярном виде. Характерной особенностью этого вида вакцины считается то, что главным её компонентом являются ослабленные штаммы возбудителя инфекции, способные размножаться, однако генетически лишённые вирулентности (способности заражать организм). Они способствуют выработке организмом антител и иммунной памяти.
Преимущество живых вакцин состоит в том, что ещё живые, но ослабленные возбудители побуждают человеческий организм вырабатывать длительную невосприимчивость (иммунитет) к данному патогенному агенту даже при однократной вакцинации. Существует несколько способов введения вакцины: внутримышечно, под кожу, капли в нос.
Недостаток — возможна генная мутация патогенных агентов, что приведет к заболеванию привитого. В связи с этим противопоказана для пациентов с особо ослабленным иммунитетом, а именно для людей с иммунодефицитом и онкобольных. Требует особых условий транспортировки и хранения препарата с целью обеспечения сохранности живых микроорганизмов в нём.
Особенности поствакцинального иммунитета
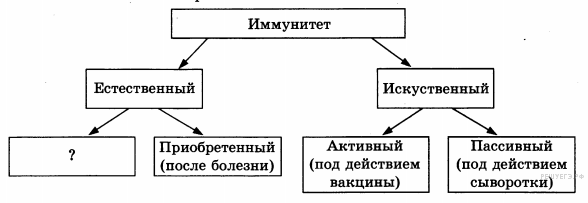
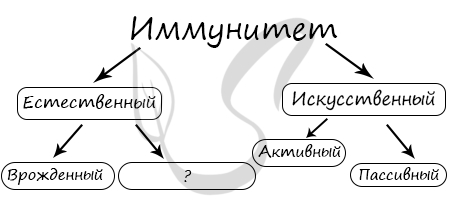
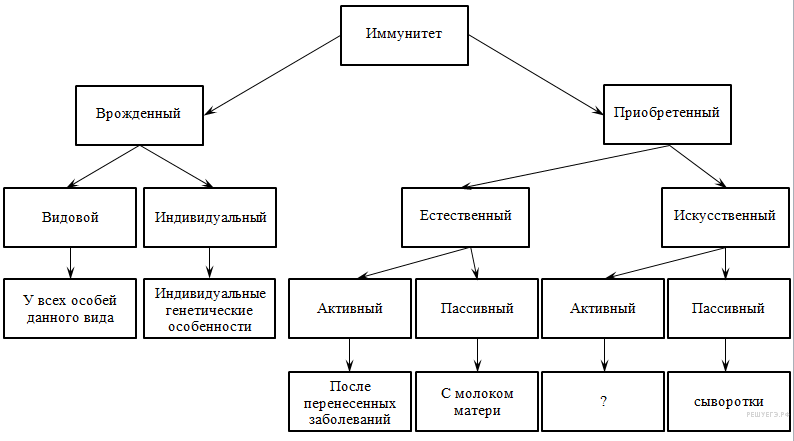
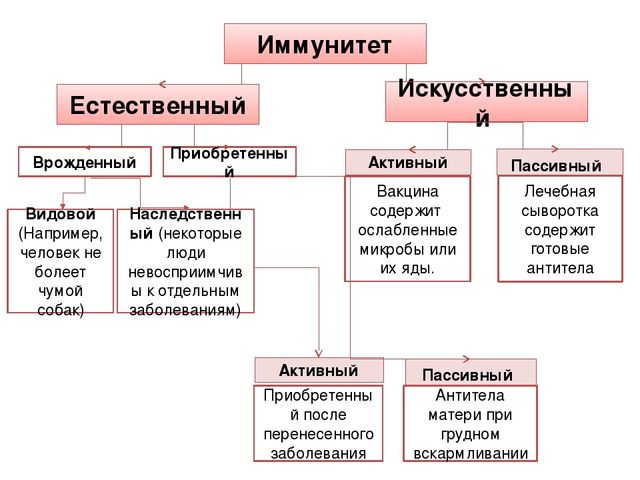
После тех или иных прививок, у человека вырабатывается иммунитет специфичный по отношению к введенным инфекционным возбудителям, формируется невосприимчивость к ним. Основными характеристиками иммунитета, возникшего от вакцины, считаются:
- выработка антител к специфичным антигенам инфекционного заболевания;
- формирование иммунитета через 2 – 3 недели;
- поддержание способности клеток длительно сохранять информацию, отвечать реакцией при выявлении гомогенного антигена;
- пониженная невосприимчивость к инфицированию при сравнении с иммунитетом, образованным после перенесенного заболевания.
Иммунитет, приобретенный человеком посредством прививок, не наследуется, при грудном кормлении не передается. В своем становлении он проходит 3 этапа:
- Скрытый. На протяжении первых 3 дней формирование протекает латентно, без видимых изменений в иммунном статусе.
- Период роста. Длится в зависимости от препарата, особенностей организма от 3 до 30 дней. Характеризуется увеличением количества антител по отношению к возбудителю, полученному при инъекции.
- Снижения иммунитета. Постепенное уменьшение ответа от прививок штаммов.
Получить полноценный ответ на Т-зависимые антигены, возможно при соблюдении ряда условий: применять следует протективные, правильно дозированные вакцины, обеспечивающие продолжительный контакт с иммунной системой. Длительность взаимодействия обеспечивают путем создания «депо», введением суспензии по схеме с соблюдением указанных интервалов, своевременной ревакцинацией. Устойчивость организма к инфекциям обеспечивается отсутствием стрессов, ведением подвижного образа жизни, сбалансированные питанием.
Вакцинацию откладывают при высоких показателях температуры, хронических заболеваниях в обостренной фазе, воспалительных процессах, иммуннодефиците, гемобластозе. Следует оценить риски вакцинации при планировании и в период беременности, аллергических состояниях при введении предыдущих вакцин.
Способы вакцинации
Иммунобиологические препараты могут вводиться различными способами согласно инструкции к вакцинам в зависимости от вида препарата. Бывают следующие способы вакцинации.
Введение вакцины внутримышечно. Местом прививки у детей до года является верхняя поверхность середины бедра, а детям с 2 лет и взрослым предпочтительнее вводить препарат в дельтовидную мышцу, которая находится в верхней части плеча. Способ применим, когда нужна инактивированная вакцина: АКДС, АДС, против вирусного гепатита В и противогриппозная вакцина.
Отзывы родителей говорят о том, что дети младенческого возраста лучше переносят вакцинацию в верхнюю часть бедра, нежели в ягодицу. Этого же мнения придерживаются и медики, обуславливая это тем, что в ягодичной области может быть аномальное размещение нервов, встречаемое у 5 % детей до года. К тому же в ягодичной области у детей этого возраста имеется значительный жировой слой, что увеличивает вероятность попадания вакцины в подкожный слой, из-за чего снижается эффективность препарата.
Подкожные инъекции вводятся тонкой иглой под кожу в области дельтовидной мышцы или предплечья. Пример — БЦЖ, прививка от оспы.
- Интраназальный способ применим для вакцин в форме мази, крема или спрея (прививка от кори, краснухи).
- Пероральный способ — это когда вакцину в виде капель помещают в рот пациенту (полиомиелит).
Трудности при разработке вакцин
Одной из главных проблем при создании вакцин является изменчивость патогенов. Самым известным примером является вирус иммунодефицита человека. ВИЧ — это ретровирус. Попадая в клетку, он переводит свою геномную РНК в ДНК посредством обратной транскрипции и встраивает ее в ДНК клетки. Обратная транскриптаза крайне «неаккуратный» фермент, который делает много ошибок, в результате чего в организме при каждом цикле размножения формируется значительное количество мутантных (измененных) форм вируса, против которых наш иммунитет, сформированный на предыдущем этапе, является неэффективным. То есть создается ситуация, когда иммунитет постоянно не успевает за изменяющимся вирусом.
Другой проблемой является низкая иммуногенность антигенов в инактивированном, например, формальдегидом возбудителе. Это наряду с невозможностью получить аттенуированную форму возбудителя (большинство возбудителей особо опасных инфекций) значительно затрудняет процесс получения вакцин.
Крайне трудно разработать вакцину против возбудителей, имеющих сложный жизненный цикл. Например, малярийный плазмодий за свой жизненный цикл сменяет несколько форм, которые очень отличаются друг от друга по строению и антигенному составу. Идентифицировать протективные антигены в этих формах или в какой-то из них и индуцировать устойчивый защитный иммунный ответ до сих пор не удается.
Иногда сложность при создании вакцины заключается в стратегии выживания патогена. Например, он может прятаться внутри клеток и убирать с их поверхности молекулы, ответственные за презентацию антигенов иммунным клеткам, тем самым становясь незаметным для уже сформированных в организме иммунных клеток (Т-клеток).
С проблемой блокировки Т-клеточного иммунитета ученые столкнулись при разработке не только противоинфекционных вакцин, но и вакцин от рака. Первые попытки создания противораковых вакцин были связаны с появлением методов выделения и накопления дендритных клеток и Т-киллеров в больших количествах. Т-киллеры стали выращивать в лабораторных условиях в присутствии опухолевых клеток, тем самым обучая их распознавать опухолевый антиген. В организм вводили такие обученные Т-киллеры либо дендритные клетки, нагруженные опухолевыми антигенами, чтобы специфические Т-лимфоциты созревали в организме. Но даже если вначале наблюдалась регрессия опухоли, вскоре она возвращалась. Было абсолютно непонятно почему. Ведь иммунитет потенциально может «выжечь» абсолютно все. Например, если формируется аутоиммунный процесс, человек может остаться без органа, к которому сформировался аутоиммунитет.
Оказалось, что опухолевые клетки умеют целенаправленно блокировать иммунный ответ в опухолевом очаге. В организме есть Т-регуляторные клетки, которые предотвращают развитие аутоиммунитета. Как только против собственных клеток развивается избыточный иммунитет, Т-регуляторные клетки соединяются определенными молекулами с рецепторами на Т-лимфоцитах и выключают их активность. Опухолевые клетки тоже умеют экспрессировать на своей поверхности такие молекулы. Получается, с собственным иммунитетом борются одновременно Т-регуляторные клетки и опухолевые клетки, и в таких условиях победить опухоль очень сложно.
Решение пришло, когда были обнаружены два ключевых рецептора: CTLA-4 и PD-1. Было показано, что введение в организм антител против них или против их лигандов пробуждает Т-лимфоциты и стимулирует противоопухолевый иммунитет (1994). Сегодня при некоторых типах рака достаточно введения таких антител без всякой химиотерапии для устойчивого увеличения показателя трехлетней выживаемости.
Успехи в борьбе со злокачественными новообразованиями еще раз подчеркивают тот факт, что для разработки эффективных вакцин необходимо детально понимать не только механизмы формирования иммунитета, но и механизмы взаимодействия конкретного патогена с иммунной системой человека.
На долгую память
У всех дочерних клеток, образовавшихся от нашедших свою мишень лимфоцитов, материнский рецептор немного изменен случайным образом, чтоб узнавание антигена было еще более точным, а связь с рецептором — прочней. Когда микроб удален, такое количество активированных лимфоцитов уже не нужно, и, получив специальные сигналы, эти клетки в большинстве своем умирают. Но их небольшое количество остается жить в течение долгого времени, иногда и на всю жизнь человека. Эти клетки называются B-клетками и Т-клетками памяти. И если тот же самый (или близкий по строению антигенов) микроб проникнет в организм еще раз, иммунный ответ на него будет в разы сильней и быстрей, потому что антигены встретятся уже с готовыми клетками памяти. А за счет вторичного изменения клеточных рецепторов они смогут опознать даже мутировавший микроб или его родственный вид, это свойство называется кросс-реактивностью. В итоге всех этих настроек болезнь, вызванная микробом, протекает гораздо легче, чем впервые возникшая, а может пройти вообще без симптомов, если возбудитель будет отловлен и обезврежен в самые первые часы. Именно этот механизм и используется при вакцинации.
Классификация вакцин и их характеристика
Медицинская микробиология позволяет выполнить классификацию вакцин согласно составу препарата. Определение прививочного препарата помогает понять суть его действия и учесть особенности формирования иммунитета. При этом виды вакцин определяют их эффективность.
Укрупнённая классификация вакцинных препаратов, в зависимости от формы действующего вещества, выглядит следующим образом. Различают вакцины:
- цельноклеточные – включают цельные микроорганизмы в ослабленной или инактивированной формах;
- бесклеточные – в отличие от предыдущей классификационной группы, содержат продукты жизнедеятельности микроба (токсины);
- корпускулярные – инфекционные агенты, входящие в состав препарата, входят в формулу препарата в цельной форме, но были предварительно убиты;
- рекомбинантные – об этих искусственных структурах, полученных при помощи генной инженерии, будет подробно рассказано ниже.
Живые
В группу живых вакцин входят препараты, в составе которых содержится ослабленный штамм патогенных бактерии или вируса. Они лишены вирулентности, но специфическая антигенность сохранена. Препараты, включающие ослабленных инфекционных агентов, называют аттенуированными.
К преимуществам живых вакцин можно отнести формирование устойчивого иммунитета, так как штаммы после введения размножаются и циркулируют в организме. Полноценный иммунный ответ вызывается на системном, локальном, клеточном и иммуноглобулиновом уровнях. Положительной стороной прививки живой вакциной является и то, что для вакцинации достаточно небольшой дозы препарата и, как правило, достаточно единоразового введения.
Однако у живых вакцин есть недостатки – высокая вероятность развития побочных эффектов, связанная с наличием в препарате большого количества реактогенов. Вакцина данного вида не может быть поставлена пациенту, у которого был выявлен иммунодефицит.
Инактивированные
В состав инактивированных вакцин входят убитые физическим или химическим способом культуры вирусов или бактерий. Иногда их заменяют на комплекс антигенов, извлечённых из патогенных микробов. Из преимуществ стоит отметить более лёгкую реакцию организма на введение препарата, возможность вакцинации людей с иммунодефицитом.
К недостаткам инактивированных прививочных средств относят большое количество дополнительных компонентов в составе препарата.
Анатоксины
Данный вид вакцин обладает антигенными и имунногенными свойствами, но при этом лишён токсичных свойств. Культуры бактерий для препарата выращиваются в жидкой питательной среде, а затем проходят фильтрацию для удаления из состава микробных тел. Анатоксины отличаются быстротой формирования пассивного иммунитета после введения вакцины, редко вызывают побочные реакции.
Конъюгированные
Конъюгированные вакцины представляют собой комплекс токсинов и бактериальных полисахаридов. То есть изначально из возбудителей инфекции выделяются полисахариды, а затем к ним добавляют белковый носитель. За счёт этого значительно увеличиваются имунногенные свойства первых, а риск развития побочных эффектов сводится к минимуму. Благодаря низкой аллергенности конъюгированные вакцины можно применять у детей возрастом от двух месяцев.
Субъединичные
Для создания субъединичных вакцин из клеток микробов или структуры вируса выделяется компонент, провоцирующий заболевание. Это могут быть отдельный протективный белок, рибосома, ДНК и другие элементы. К преимуществам субъединичных вакцин причисляют их безопасность, низкую реактогенность, отсутствие риска развития вакциноассоциированных патологий после введения препарата.
Из недостатков стоит отметить более слабый ответ иммунитета по сравнению с иммунитетом, сформированным живыми вакцинами. В расчёт также стоит брать и то, что для формирования стойкой защиты требуется ревакцинация, единоразового введения препарата недостаточно.
Рекомбинантные векторные вакцины
Препарат изготавливается по методу генной инженерии. Его суть заключается в том, что генетический материал патогенного микроорганизма искусственным путем встраивается в дрожжевые клетки, продуцирующие антиген. Затем доросшие до определённого значения клетки очищают, выделяя из них антиген, и проводят очистку компонента препарата. Рекомбинантные векторные вакцины отличаются высокой эффективностью и практически нулевым процентом вероятности развития побочных эффектов.
Кроме классификации по составу, вакцины различаются по способу производства, назначению, методам применения.
Какие вакцины относятся к живым: полный перечень
Эпидемические вспышки брюшного тифа, кори, краснухи, полиомиелита, эпидемического паротита, зафиксированные в странах Европы и Северной Америки во второй половине 20-го столетия, определили вектор медицинских исследований в то время. В результате таких изысканий, уже к началу 70-х годов врачи оперировали тремя десятками живых вакцин.
Не во всех случаях применяют живые вакцины. Однако перечень болезней, от которых ними прививают, широк и включает такие инфекции, как:
- полиомиелит;
- туберкулёз;
- паротит;
- оспа;
- корь;
- бешенство;
- грипп;
- туляремия;
- сибирская язва;
- чума;
- краснуха;
- некоторые виды лихорадок.
В списке – обязательные прививки, предусмотренные календарём, и те, которые ставят по желанию.
На какое время сохраняется иммунный ответ, возникающий путем иммунизации?
Многие пациенты интересуются, на какое время сохраняется иммунный ответ, возникший в результате вакцинации. Все зависит от типа и качества прививки, введенной дозы, особенностей организма, наличия протективных антигенов, возраста человека.
профилактики гриппа
Вакцина против коревой болезни для детей действует около 5-5,5 лет, а для взрослых, прошедших полный курс прививок, – примерно 20 лет.
Вакцинирование против свинки, краснухи и кори детям обеспечивает защиту на 5-6 лет, а взрослым – на 10 и более лет. У некоторых мужчин и женщин иммунный ответ сохраняется в течение всей жизни.
После прохождения курса иммунопрофилактики гепатита В, человек становится защищенным на 20-25 лет. После укола АКДС первичный иммунный ответ наблюдается в течение 1,5-2 месяцев.
После трехкратного введения препарата защита сохраняется в течение 8 месяцев. Далее для поддержки крепости детям вводят АКДС в 6 и 14 лет. У взрослых иммунный ответ отмечается на протяжении 10 лет.
Что такое живая вакцина
Живая вакцина – препарат, который используют для иммунизации. В его составе – обезвреженные штаммы микроорганизмов, вызывающих болезнь, они начинают распространяться в месте укола. Заболевание не прогрессирует, однако иммунитет формируется, причём стойкий – гуморальный, клеточный и секреторный.
Ослабленные штаммы получают в процессе деактивации гена, отвечающего за заразность бактерии. Обезвреживания добиваются различными способами – химическими или физическими (например, воздействием высоких температур). Обычно живые вакцины представляют собой порошок, который растворяют в жидкости для инъекции. Сухие препараты хранятся дольше и не повреждаются при транспортировке. Однократное введение средства способствует выработке иммунитета.
Одним из видов живых вакцин являются дивергентные. Они изготавливаются из микроорганизмов, находящихся в близком родстве с возбудителем инфекции, но вызвать заболевание не могут. Самый яркий пример подобного препарата – БЦЖ, в основе средства – бактерии не человеческого, а бычьего туберкулёза.
Глобализация применения вакцин
Каждый гражданин должен понимать, что предотвратить распространение инфекции можно лишь профилактическими мероприятиями, которые отражены в календаре прививок отдельно взятого государства. В документе указана информация о перечне вакцин, эпидемиологически оправданных для конкретной территории, сроках их постановки.
ВОЗ создала расширенную программу иммунизации (РПИ) в 1974 году, направленную на предупреждение возникновения инфекций, сокращение их распространения.
Благодаря РПИ выделяют несколько значимых этапов, позволивших сократить возникновение очагов ряда заболеваний:
- 1974 – 1990 гг. – активная иммунизация против кори, столбняка, полиомиелита, туберкулеза, коклюша;
- 1990 – 2000 гг. – ликвидация краснухи беременных, полиомиелита, столбняка новорожденных. Снижение инфицирования корью, свинкой, коклюшем, параллельная разработка, применение суспензий, сывороток против японского энцефалита, желтой лихорадки;
- 2000 – 2025 гг. – реализуется введение ассоциированных препаратов, планируется ликвидация дифтерии, краснухи, кори, гемофильной инфекции, паротита.
Масштабный охват вызывает некоторые опасения со стороны населения, среди молодых родителей, опасающихся мельчайших признаков нездоровья ребенка. Следует помнить, что средства, формирующие иммунитет, защитят от специфичных заболеваний, предотвратят осложнения, патологические изменения, смерть при инфицировании в ситуациях отказа от прививки. Даже здоровый образ жизни не способен обезопасить организм от воздействия вирусов, бактерий.
В случаях заражения после прививки, например при ненадлежащем хранении средства, нарушениях введения препарата, болезнь протекает легко и без последствий, благодаря наличию иммунитета. Плановая вакцинация экономически оправдана, так как лечение в случае инфицирования потребует больше средств, чем стоимость вакцины.