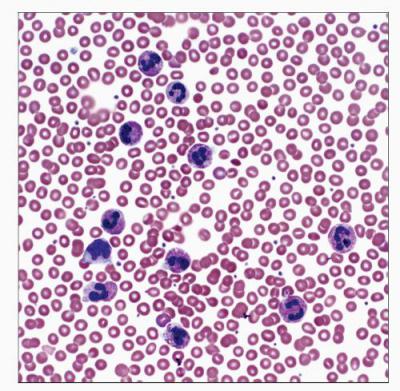
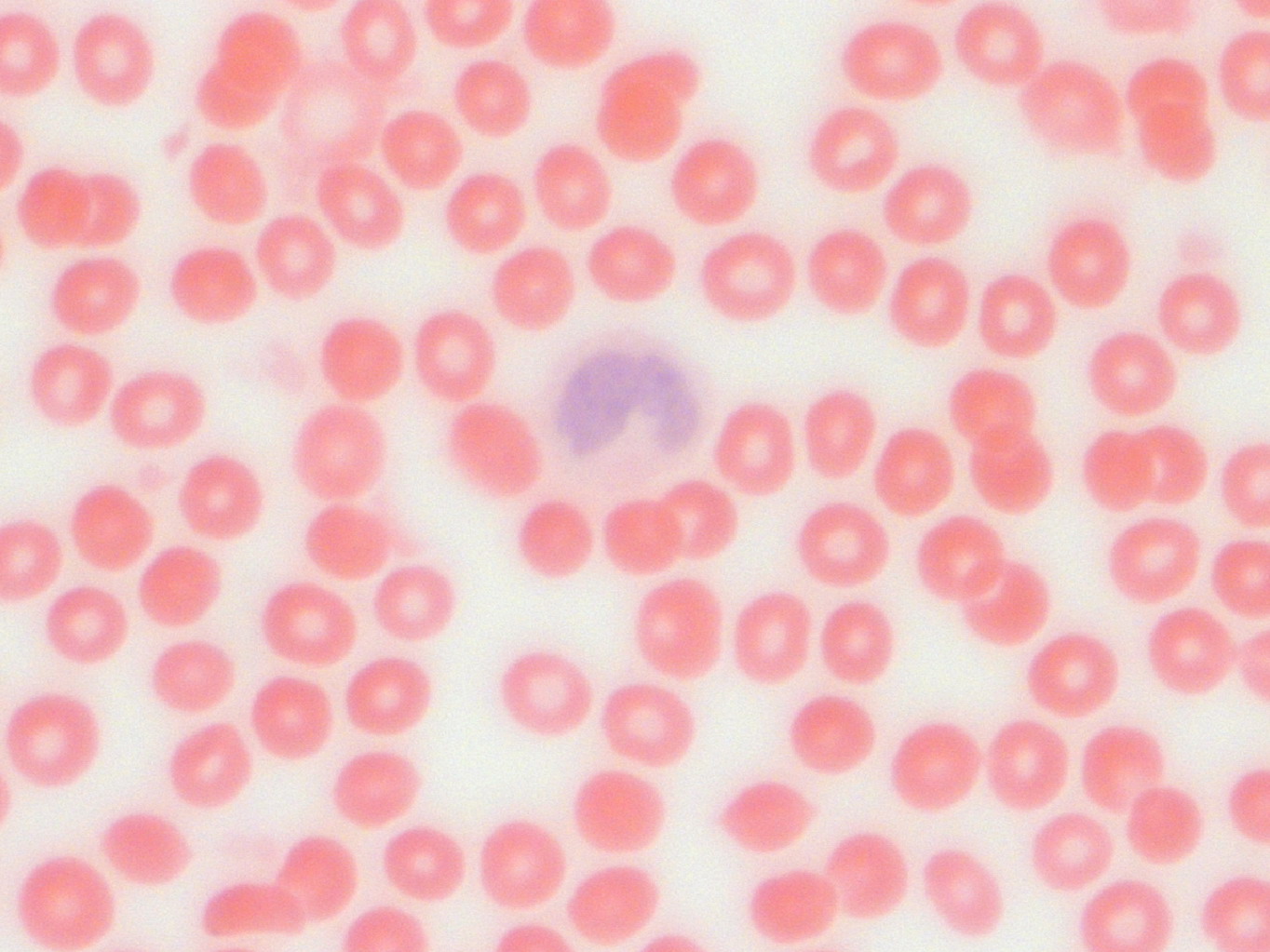
Нейтрофильные гранулоцииты
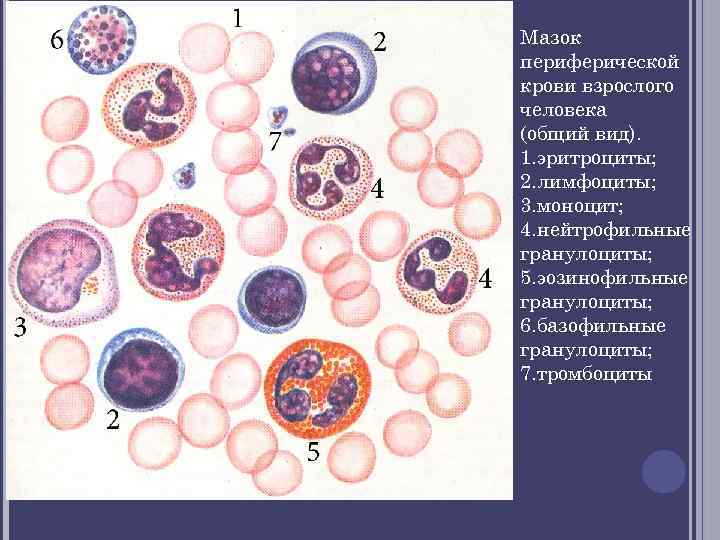
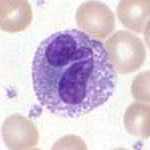
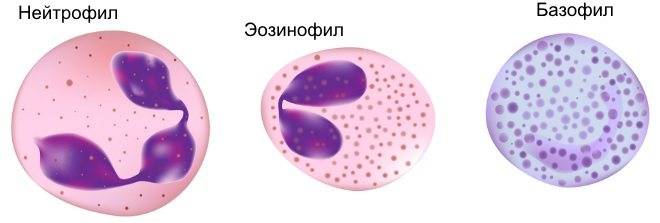
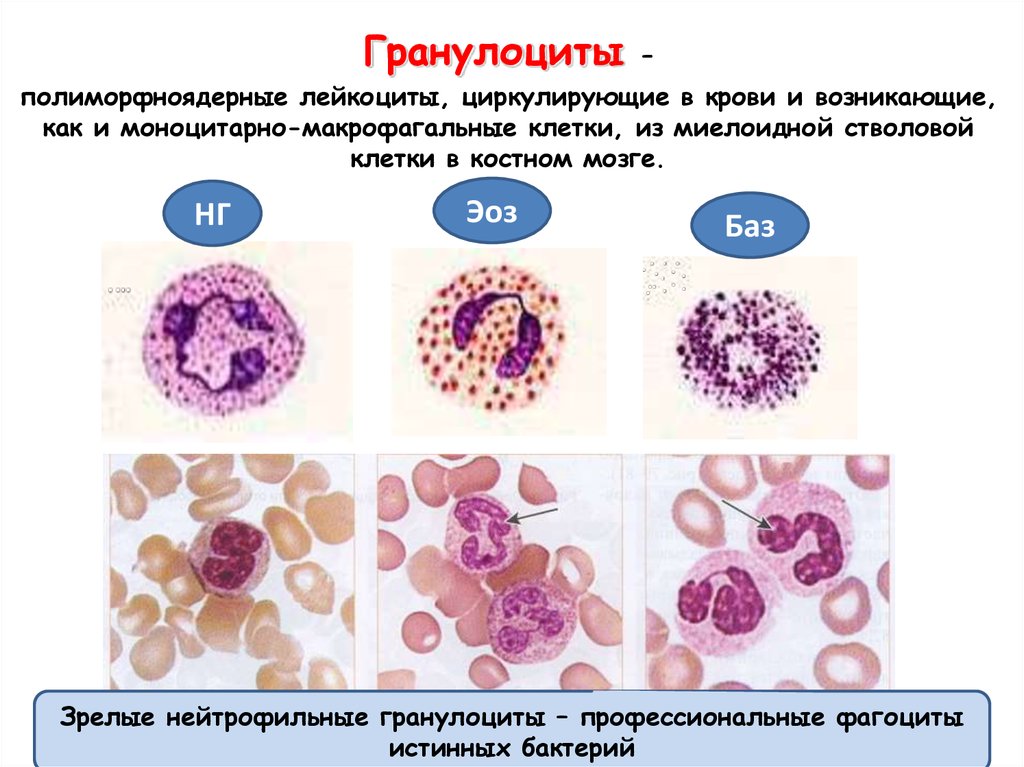
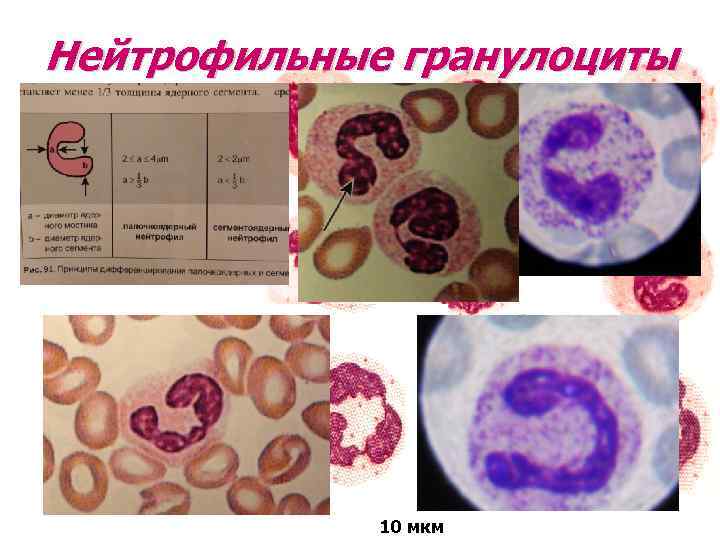
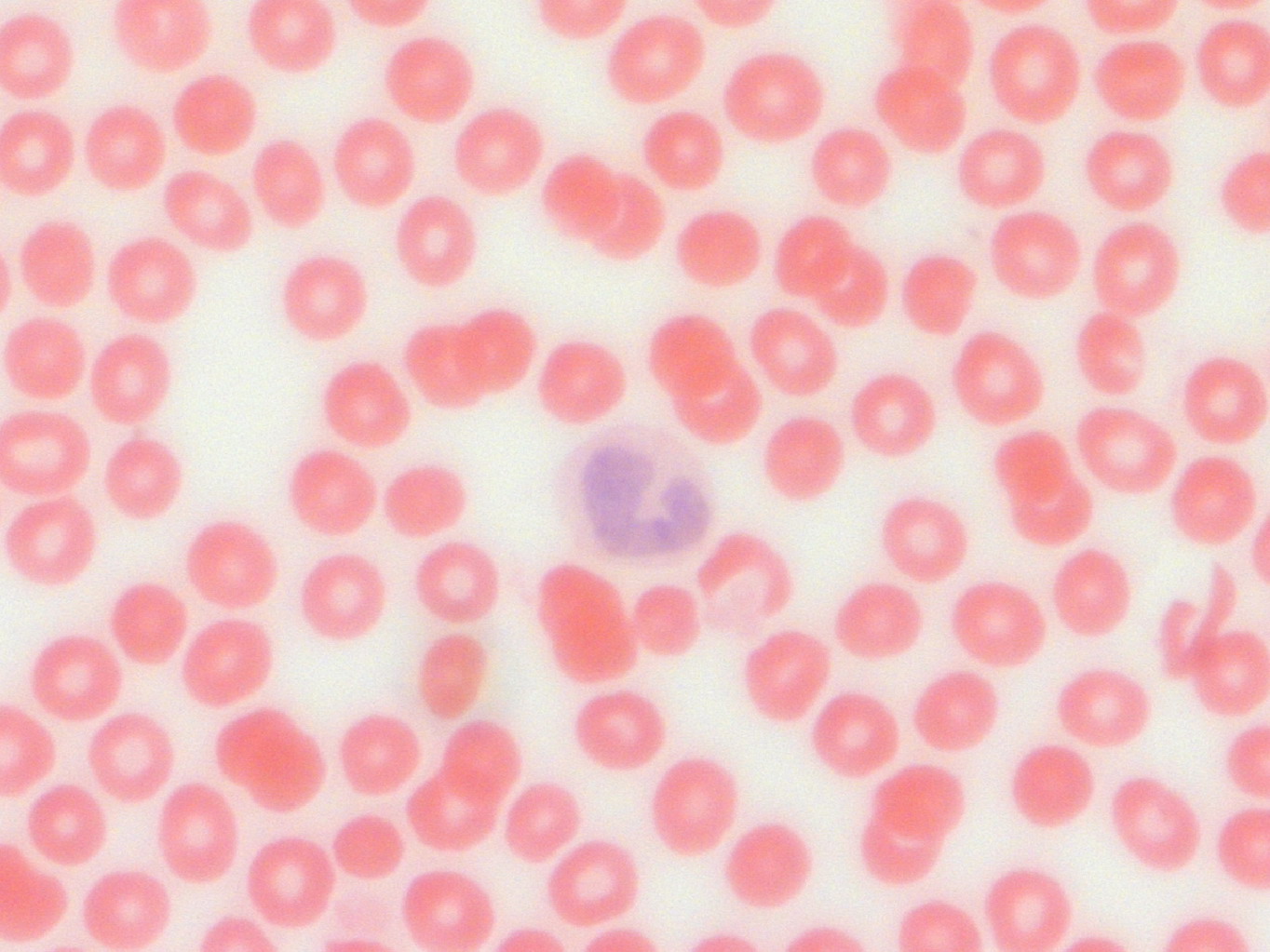
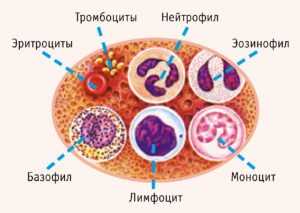
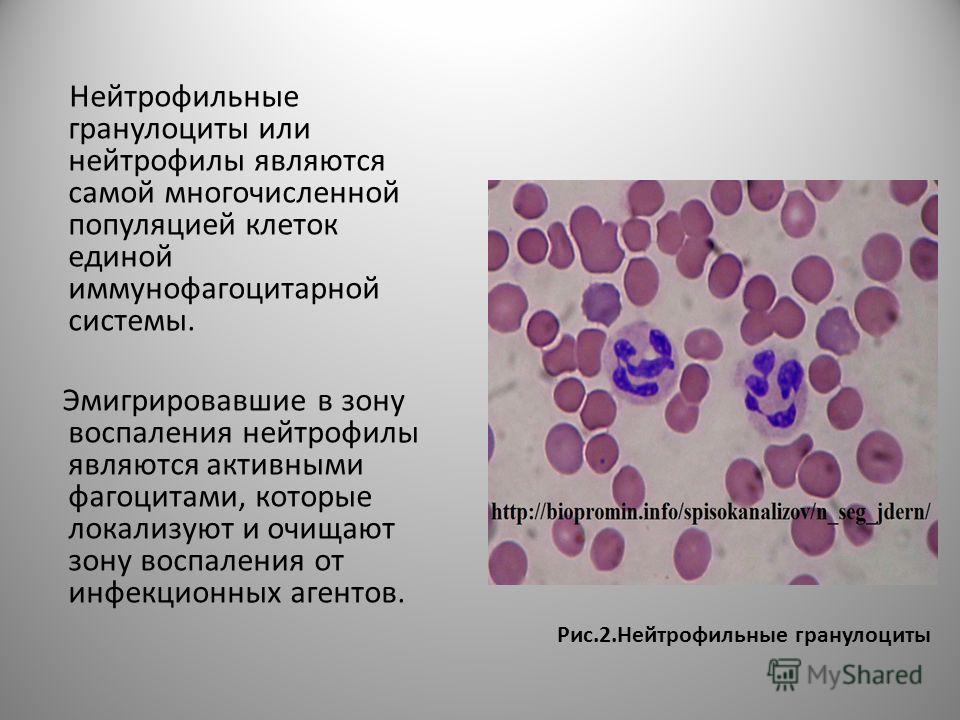
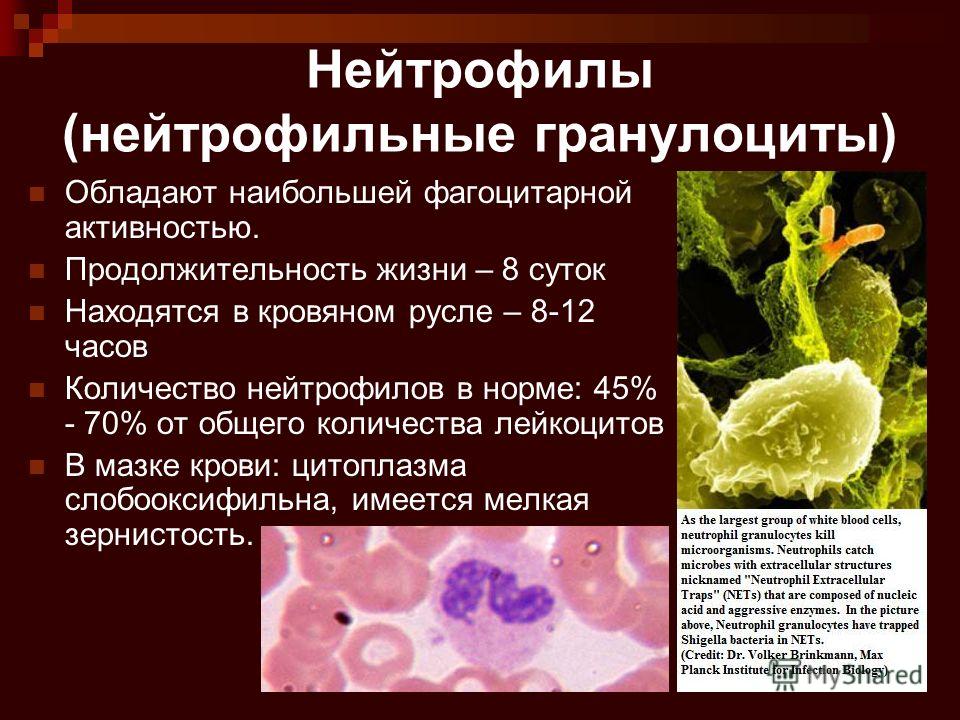
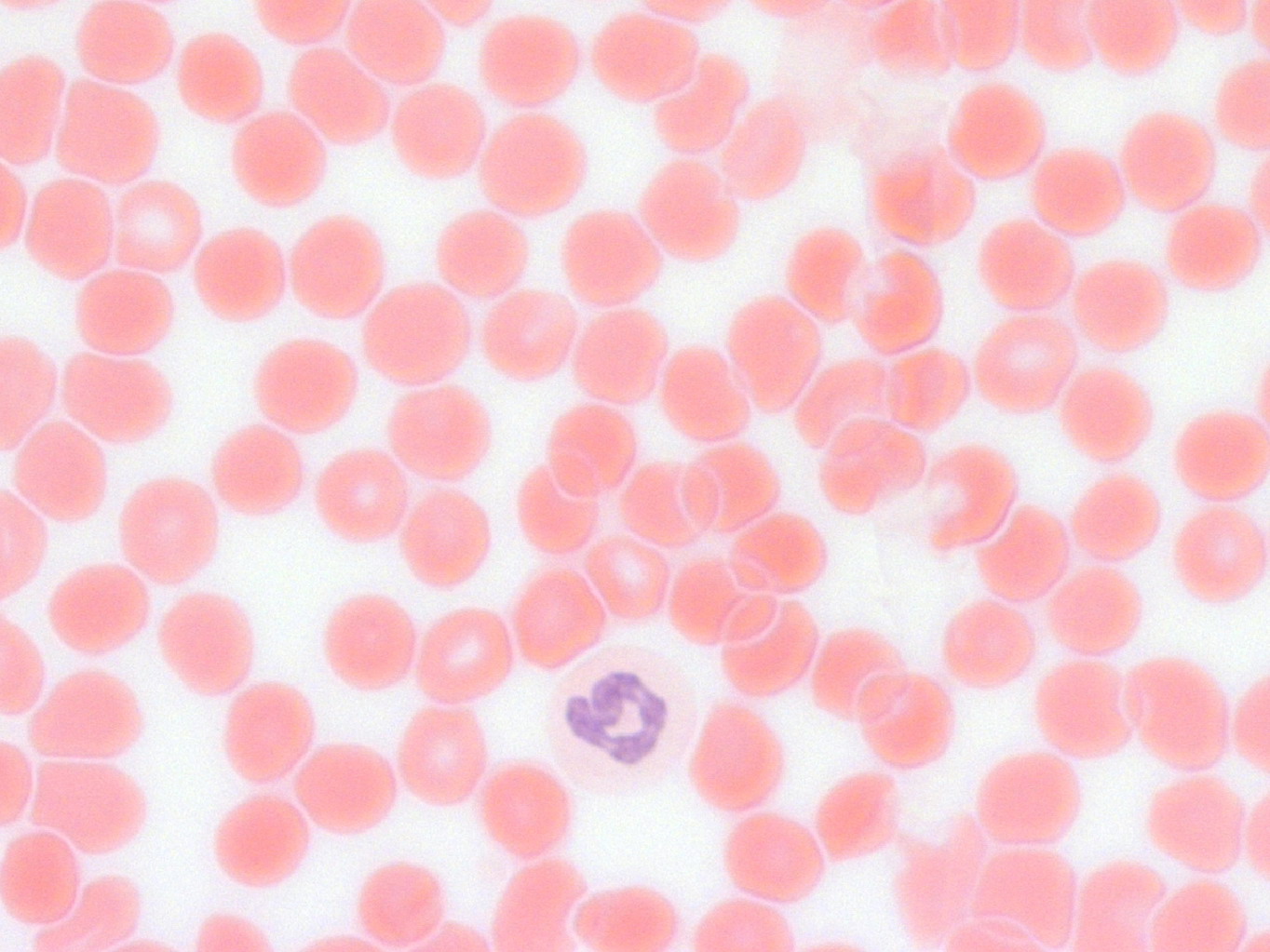
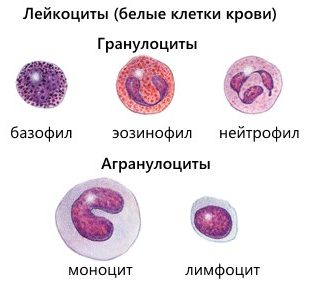
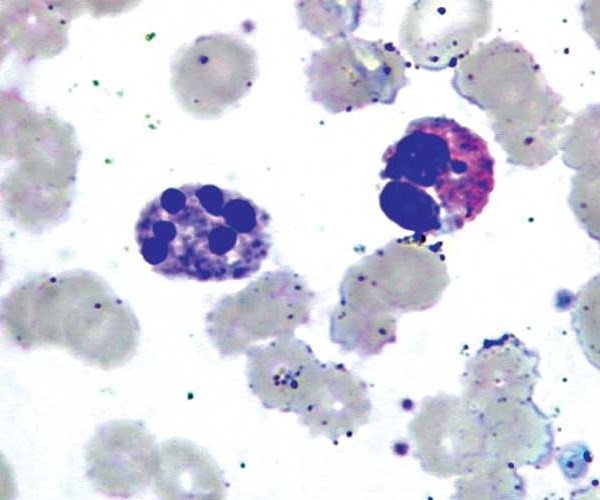
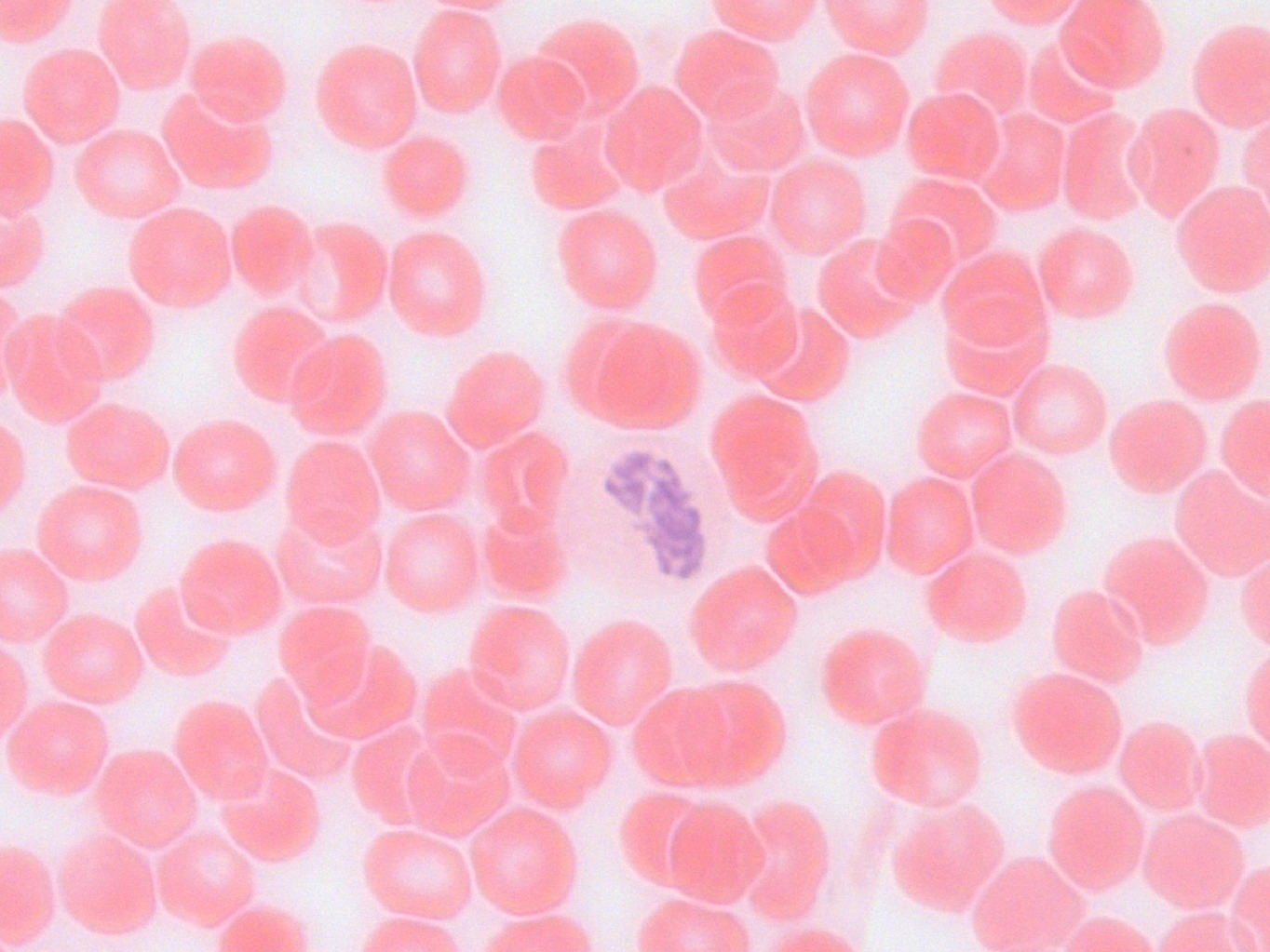
Нейтрофильные гранулоциты (нейтрофилы) клетки белой крови. Это вид лейкоцитов, который содержит в цитоплазме гранулы, а потому называются гранулоциты. Нейтрофильными они называются потому, что при окрашивании кислыми и основными красителями гранулы окрашены в нейтральный розовый цвет, тогда как базофилы и эозинофилы (другие лейкоциты), окрашены темно-синий и ярко-красный цвета соответственно. Ядро нейтрофилов состоит из нескольких сегментов, поэтому их называют сегментоядерные нейтрофилы.
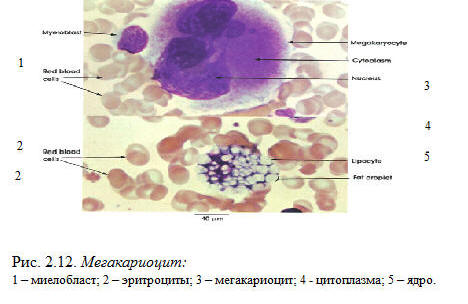
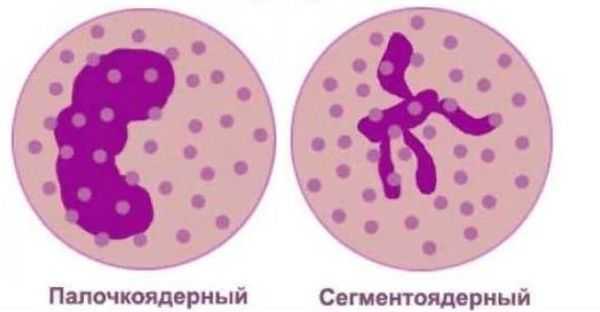
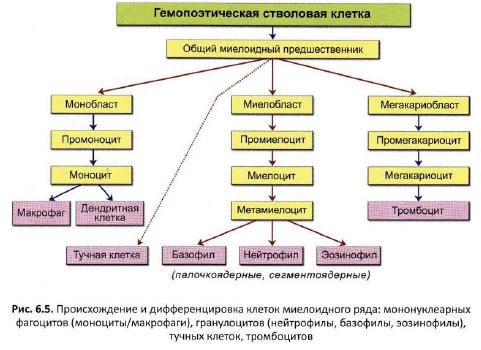
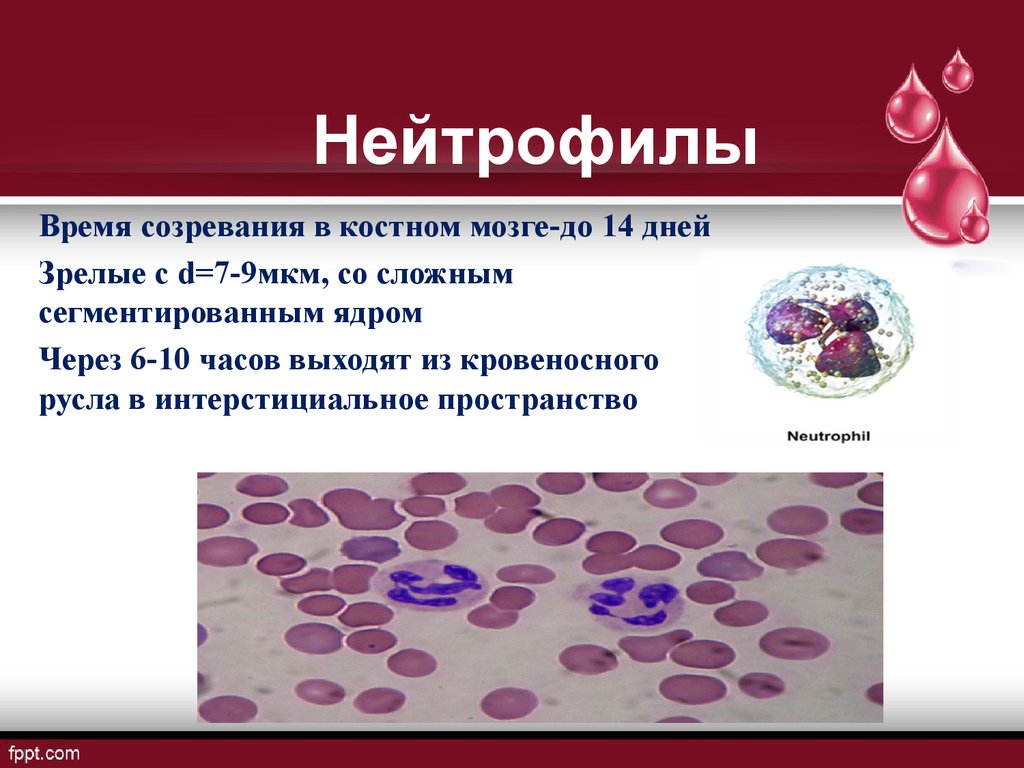
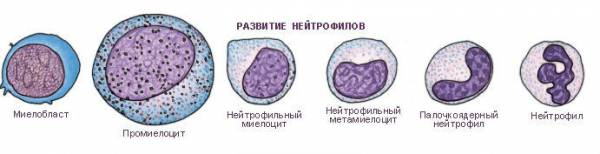
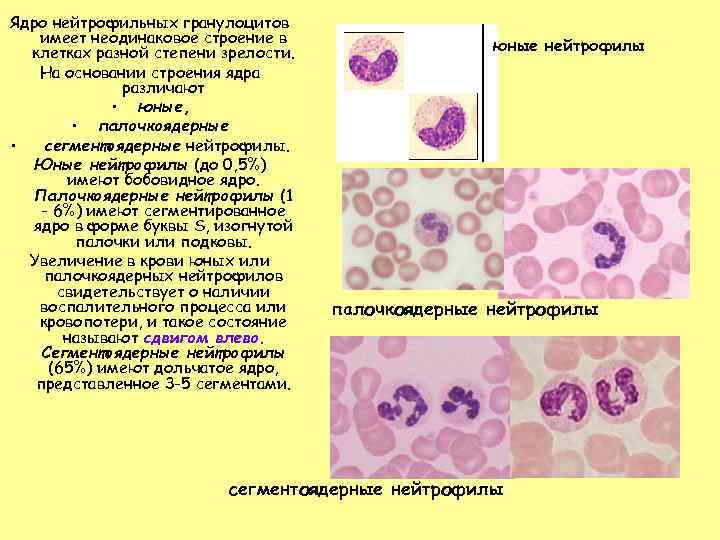
Созревают нейтрофильные гранулоциты в костном мозге. За время созревания они проходят шесть стадий развития, в соответствии с которыми их называют миелобласты, промиелоциты, миелоциты, метамиелоциты, палочкоядерные и сегменттоядерные. Нейтрофилы первых четырех стадий развития в норме в циркуляции отсутствуют, клетки пятой и шестой стадий (сегментоядерные и палочкоядерные) всегда присутствуют в крови Палочкоядерные нейтрофилы, в отличие от сегментоядерных — незрелая форма нейтрофильных гранулоцитов. Время созревания нейтрофилов в костном мозге — от 11 до 14 дней. При отсутствии воспалительных процессов продолжительность жизни нейтрофилов в крови составляет 6 — 7 часов. При воспалительных процессах нейтрофильные гранулоциты мигрируют в ткани, где живут несколько дней.
При нормальном гомеостазе нейтрофилы составляют 50-70% общего количества лейкоцитов, с абсолютным числом приблизительно 55 х 106 клеток на кг массы тела взрослого человека. Ежедневно в кровоток поступает 1011 клеток/24 часа или 1,1х 106 клеток/секунду! В условиях острого воспаления поступление нейтрофилов из костного мозга значительно увеличивается. Нейтрофильные гранулоциты содержат 4 типа гранул. Каждый тип гранул содержит специфические ферменты и белки, последовательное освобождение которых обеспечивает направленную миграцию нейтрофилов в очаг воспаления и способность разрушить любую структуру, которую поглощают нейтрофилы. Одна из основных функций нейтрофилов — поглощение возбудителей -фагоцитоз.
Нейтрофильные гранулоциты: абсолютное содержание
Абсолютное количество нейтрофилов (АКН) — содержание клеток в 1 микролитре (мкл) или 1 кубическом миллилитре (мм3) рассчитывается на основании общего числа лейкоцитов и процентного содержания нейтрофильных гранулоцитов. AКН позволяет судить о степени риска инфекций.. Нормальный диапазон АКН выше 1500 клеток / мкл, значение ниже 500 клеток / мкл считается низким и оценивается как нейтропения. Нейтропения может быть врожденной или приобретенной (побочные эффекты лекарственных препаратов, таких как химиотерапия). Нейтропения — отражение ослабленной иммунной системы, показатель риска высокой восприимчивости к инфекции. Наличие нейтропении обязывает к проведению надлежащей терапии, в отсутствие которой может быть сепсис (опасное для жизни состояние).
Нейтрофильные гранулоциты: роль в воспалении
Нейтрофильные гранулоциты несут ответственность за защиту нашего организма от инфекций. Они включаются в защиту в ответ на любой тип повреждающего воздействия: физические (тепло, холод, стресс), химические (лекарства) и биологические (болезнетворные организмы). Нейтрофилы первыми встречают патоген при проникновении его в организм через физико-химические барьеры (кожу, слизистые).
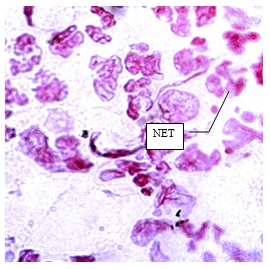
В начальной стадии воспаления нейтрофильные гранулоциты мигрируют из крови к месту локализации патогена посредством процесса, известного как хемотаксис (химические сигналы, которые посылаются поврежденными клетками или микроорганизмами называются хематтрактанты). Нейтрофилы воспринимают сигнал хематтрактантов и в пределах одного часа перемещаются в очаг воспаления. Нейтрофильные гранулоциты могут «расправляться» с возбудителями двумя путями: поглощая их (фагоцитоз) и переваривания внутри клетки с помощью содержимого гранул Это внутриклеточный механизм киллинга бактерий нейтрофильными гранулоцитами. Второй путь киллинга бактерий нейтрофильными гранулоцитами — образование внеклеточных ловушек (NETs): нейтрофилы выбрасывают ядерный материал в виде нитей ДНК вместе с гранулами; нити образуют сетку, которая «отлавливают» и уничтожает бактерии. Как солдат иммунной системы, нейтрофильный гранулоцит — клетка-камикадзе: выполнив свою функцию подвергается апоптозу.
Антимикробные функции
Нейтрофилы обладают большим набором антибиотических белков, которые хранятся в гранулах двух типов. Первичные (азурофильные) гранулы — это лизосомы, содержащие кислые гидролазы, миелопероксидазу и мурамидазу (лизоцим). Во вторичных (специфических) гранулах дополнительно к лизоциму обнаружен лактоферрин. Кроме ферментов и лактоферрина, в этих гранулах содержатся в высоких концентрациях антибиотические белки — дефензины, сепроцидины, кателицидины и белок, индуцирующий проницаемость бактериальных клеток.
Нейтрофилы играют очень важную роль в защите организма от бактериальных и грибковых инфекций, и сравнительно меньшую — в защите от вирусных инфекций. В противоопухолевой или антигельминтной защите нейтрофилы практически не играют роли.
Функции ABS-клеток
Все функционирование нейтрофильных гранулоцитов направлено на борьбу с бактериями (к другим патогенам нейтрофилы практически равнодушны). Это осуществляется несколькими путями:
- Фагоцитоз;
- Стимулирование иммунитета;
- Нетоз.
Принципы фагоцитоза
Фагоцитоз – это явление захвата, «окутывания» (подобно действию амёбы) и переваривания чужеродной бактерии нейтрофильными лейкоцитами. Гранулы нейтрофилов содержат множество лизосомных ферментов, которые и осуществляют расщепление белков чужеродных тел. После такой интенсивной атаки сама клетка-защитница погибает, но успевает уничтожить порядка 7 микроорганизмов. По своей сути эта группа кровяных телец является самоубийцами (камикадзе), которые жертвуют собой ради здоровья всего организма.
Эта особенность клеток напрямую указывает на способность организма бороться с инфекцией. В анализе крови на качество работы иммунитета есть такой показатель – «фагоцитарная активность нейтрофилов», он указывает, сколько чужеродных микроорганизмов «съели» клетки-камикадзе, содержащиеся в 1 мл крови, за определённый промежуток времени в условиях лаборатории. Это важный диагностический критерий.
Механизмы стимулирования иммунитета
Процесс выработки антител начинается только после «съедания» патогенна нейтрофильными гранулоцитами. После расщепления на составляющие информация о чужеродном микроорганизме, становится доступной для каждой кровяной клетки и иммунной системы в целом. Она начинает интенсивно работать, активизирует защитные механизмы, формирует антитела, направляет ещё больше клеток-защитников к очагу обнаружения «вредителя».
Особенности нетоза
Нетоз – ещё один важный механизм работы нейтрофилов, открытый только в 2004 году. Когда нейтрофильный гранулоцит обнаруживает патогенный микроорганизм, в его ядре начинаются сложные процессы: оно разрушается с образованием отдельных нитей хроматина, идёт интенсивное накопление радикалов и различных токсических веществ, препятствующих нормальному функционированию живых клеток. Гранулы клеток высвобождают ферменты и вещества с бактерицидными свойствами. Затем разрушается оболочка кровяных телец, и весь набор устремляется в межклеточное пространство. В таких условиях бактериальная клетка очень быстро погибает, а нейтрофил снова жертвует собой.
Увеличение или уменьшение количества нейтрофилов в анализах — Полисмед
Нейтрофилы и их значение в анализах: уменьшение и увеличение количества нейтрофилов в общем анализе крови, в анализе мокроты и в мазках Нейтрофилы это клетки крови из группы лейкоцитов, обеспечивающих защиту организма человека от различных инфекций. Большая часть нейтрофилов циркулирует в крови лишь несколько часов, а затем проникают в ткани и органы, которые они защищают от инфекций. Нейтрофилы способны улавливать «сигналы воспаления» и целенаправленно мигрировать к местам воспаления (раны, ожоги, травмы). Увеличение количества нейтрофилов в крови является характерным признаком инфекции и воспаления. Уменьшение количества нейтрофилов в крови наблюдается при использовании некоторых лекарств, и на фоне определенных вирусных и паразитарных болезней. Что такое нейтрофилы? Нейтрофилы, или нейтрофильные гранулоциты – это один из видов лейкоцитов, белых клеток крови, которые участвуют в поддержании иммунитета человека, и играют ключевую роль в борьбе с бактериальными инфекциями. Нейтрофилы созревают в костном мозге, высвобождаясь в кровь со скоростью примерно 7 млн. в мин. В крови нейтрофилы циркулируют от 8 часов до 2 суток, далее они мигрируют в ткани где и обеспечивают защиту от инфекций. Разрушение старых нейтрофилов происходит в тканях. В костном мозге можно наблюдать шесть последовательных стадий созревания нейтрофилов: миелобласт, промиелоцит, миелоцит, метамиелоцит, палочкоядерная и сегментоядерная клетка. Все формы нейтрофилов кроме сегментоядерной клетки являются молодыми (незрелыми). Если в организме есть инфекция или воспалительный процесс, скорость высвобождения нейтрофилов из костного мозга увеличивается и в кровь попадают незрелые нейтрофилы. По количеству незрелых клеток в крови человека можно судить о наличии бактериальной инфекции и ее активности в организме. Основная функция нейтрофилов — это фагоцитоз (уничтожение бактерий). При острых инфекционных заболеваниях число нейтрофилов быстро повышается. Они могут находиться и действовать в тканях, бедных кислородом: воспаленные ткани, ткани захваченные отеком. Нейтрофилы распознают, а затем поглощают (фагоцитируют) бактерии и продукты распада тканей и разрушают их своими ферментами. Ферменты, высвобождающиеся при распаде нейтрофилов, вызывают размягчение окружающих тканей, т.е. формирование гнойного очага (абсцесса). Гной в местах воспаления состоит главным образом из нейтрофилов и их остатков. Норма содержания нейтрофилов в крови У здорового человека количество палочкоядерных нейтрофилов (незрелая форма нейтрофилов) в крови составляет от 1 до 6% от всех лейкоцитов или 0,04-0,3 х 109/л, количество сегментоядерных нейтрофилов (зрелая форма нейтрофилов) составляет от 47 до 72% или 2,0-5,5 х 109/л. Количество нейтрофилов в крови у ребенка зависит от возраста:
- В 1-й день в крови новорожденного палочкоядерные нейтрофилы составляют от 1 до 17%, сегментоядерные нейтрофилы от 45 до 80%.
- У детей до года: палочкоядерные нейтрофилы 0,5-4% и сегментоядерный нейтрофилы 15-45%
- От 1 года до 12 лет палочкоядерные нейтрофилы 0,5-5% и сегментоядерный нейтрофилы 25-62%.У детей 13-15 лет количество палочкоядерных нейтрофилов составляет от 0,5 до 6%, сегментоядерных нейтрофилов от 40 до 65%.
Нетоз
В 2004 году был открыт важный механизм, посредством которого нейтрофилы осуществляют защитные функции, названный нетозом (от англ. NETosis (от NET — Neutrophil Extracellular Trap)).
Нетоз является третьим основным типом клеточной смерти нейтрофилов наравне с апоптозом и некрозом.
При нетозе нейтрофил проходит стадии деконденсации хроматина, наработки реактивных форм кислорода (ROS — Reactive Oxygen Species), дегрануляции; затем следует выброс ДНК-сети, связанной с ROS, гистонами, миелопероксидазой и другими молекулами, повреждающими патоген.
Патогены, а именно бактерии, грибы, паразиты и вирусы «запутываются» в сетях и гибнут.
Нейтрофильные ДНК-ловушки связаны с патогенезом различных заболеваний, таких как сепсис, ревматоидный артрит, тромбоз, волчанка и другие аутоиммунные заболевания.
Также показано, что другие клетки крови, такие как моноциты, эозинофилы, базофилы также имеют подобный механизм, называемый этозом (от англ. ETosis (от ET — Extracellular Trap)).
Нейтрофильный ответ (инфильтрация очага воспаления нейтрофилами, повышение числа нейтрофилов в крови, сдвиг лейкоцитарной формулы влево с увеличением доли «юных» форм, указывающий на усиление продукции нейтрофилов костным мозгом) — самый первый ответ на бактериальные и многие другие инфекции.
Нейтрофильный ответ при острых воспалениях и инфекциях всегда предшествует более специфическому лимфоцитарному. При хронических воспалениях и инфекциях роль нейтрофилов незначительна и преобладает лимфоцитарный ответ (инфильтрация очага воспаления лимфоцитами, абсолютный или относительный лимфоцитоз в крови).
Исход нейтрофильного воспаления
хронической гранулематозной болезни
Длительное присутствие провоспалительных цитокинов в очаге инфекционного воспаления, как правило, свидетельствует о недостаточной эффективности защитных реакций нейтрофилов. Причины этого могут быть различными: высокий уровень патогенности и большое количество инвазирующих микроорганизмов, обширная зона тканевой деструкции, недостаточный уровень опсонинов. Затяжной характер процесса при стерильном воспалении обычно связан с пролонгированным действием этиологического фактора, который может быть экзогенным (по природе — химическим или физическим) и эндогенным (отложение солей, присутствие аутоантител или иммунных комплексов).
Развитие бактериального гнойного процесса обычно является показателем дефицита опсонинов. При этом большое количество гноя отражает высокий мобилизационный резерв нейтрофилов. Однако их бактерицидная функция (важнейшим проявлением которой является внутриклеточное уничтожение микробов) оказывается недостаточной. Ярким примером развития такой ситуации является фурункулез. Введение больному антистафилококковых антител или проведение курса иммунизации стафилококковым анатоксином, как правило, дает позитивный результат. Назначение антибиотиков обычно также направлено на повышение бактерицидного потенциала организма. Необходимо подчеркнуть, что vivo антибактериальное действие фармацевтических препаратов является лишь дополнением к мощному защитному арсеналу организма и является малоэффективным при его разрушении (первичные иммунодефициты, острая лучевая болезнь, СПИД и тд.).
Затяжной характер нейтрофильного воспаления может поддерживаться самими нейтрофилами через продукцию PAF, IL-8, LTB4. Из них наиболее эффективен для притока нейтрофилов LTB4. Этот метаболит 5-липоксигеназного пути превращения арахидоновой кислоты (арахидоновая кислота высвобождается под действием фосфолипазы А2 из фосфолипидов мембраны) не только вызывает увеличение проницаемости сосудов, но и усиливает экспрессию молекул адгезии на эндотелиальных клетках, стимулирует хемотаксис и дегрануляцию нейтрофилов. Затухание воспалительной реакции обычно сопровождается подавлением продукции LTB4.
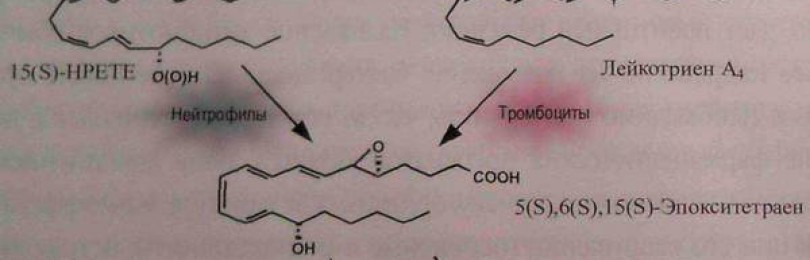
Данные, полученные Чарльзом Сераном, свидетельствуют о возможности прямого участия нейтрофилов в торможении воспалительного процесса. Известно, что нейтрофилы способны секретировать в окружающую среду лейкотриен A4 (LTA4 — метаболический предшественник LTB4), который поглощается адгезированными тромбоцитами и превращается ими в липоксины.
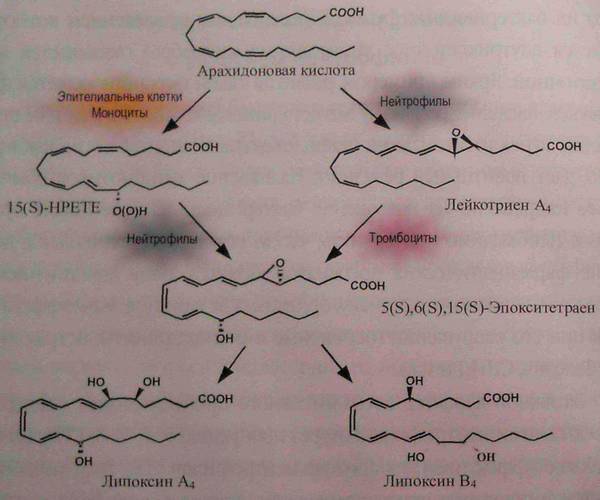
Последние представляют собой мощные противовоспалительные факторы. Образование липоксинов может также протекать в самих нейтрофилах при участии 5-липоксигеназы — ключевого фермента синтеза лейкотриенов. В этой ситуации нейтрофилы захватывают 15S-гидроксиэйкозатриеновую кислоту (15S-HETE), образуемую близлежащими эпителиальными клетками и моноцитами под влиянием цитокинов IL-4 и IL-13
Важной особенностью этого пути образования липоксинов является параллельное угнетение продукции лейкотриенов, в том числе и LTB4. Таким образом, нейтрофилы способны не только индуцировать развитие острого воспаления, но и активно участвовать в его подавлении
Шмагель К.В.
Характеристика
Зрелые нейтрофилы имеют сегментированное ядро, то есть относятся к полиморфноядерным лейкоцитам, или полиморфонуклеарам. Они являются классическими фагоцитами: имеют адгезивность, подвижность, способность к хемотаксису, а также способность захватывать частицы (например, бактерии).
Хемотаксис нейтрофилов вызывают фрагменты белков, образующиеся в результате активации комплемента, факторы фибринолитической и кининовой систем, а также продукты лейкоцитарного, тромбоцитарного и бактериального происхождения. Под действием хемотаксических стимулов происходят «краевое состояние» (прилипание к эндотелиальным клеткам) и диапедез нейтрофилов.
Зрелые сегментоядерные нейтрофилы в норме являются основным видом лейкоцитов, циркулирующих в крови человека, составляя от 47 % до 72 % общего количества лейкоцитов крови. Ещё 1—5 % в норме составляют юные, функционально незрелые нейтрофилы, имеющие палочкообразное сплошное ядро и не имеющие характерной для зрелых нейтрофилов сегментации ядра — так называемые палочкоядерные нейтрофилы.
Нейтрофилы способны к активному амёбоидному движению, к экстравазации (эмиграции за пределы кровеносных сосудов), и к хемотаксису (преимущественному движению в направлении мест воспаления или повреждения тканей).
Функции нейтрофильных гранулоцитов ( лейкоцитов ). Дефенсины. Кателицидины. Белки острой фазы. Хемотаксические факторы.
Функцией зрелых нейтрофильных лейкоцитов является уничтожение проникших в организм инфекционных агентов. Осуществляют ее они, тесно взаимодействуя с макрофагами, Т- и В-лимфоцитами
На важность функционального вклада нейтрофилов в защиту организма от инфекции указывает, например, тяжесть течения инфекционных заболеваний у больных, страдающих сниженной продукцией или качественными нарушениями этих клеток. Нейтрофилы фагоцитируют поврежденные клетки собственного организма, секретируют бактерицидные вещества и способствуют регенерации тканей, удаляя из них поврежденные клетки, а также секретируя стимулирующие регенерацию тканей вещества (нейтрофилокины)
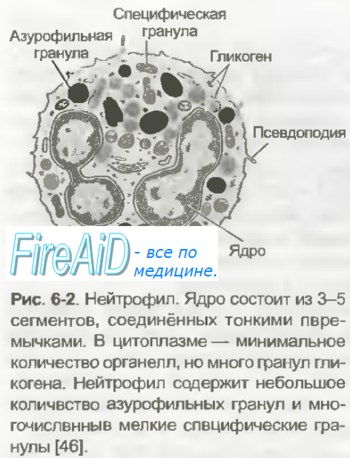
Зрелый нейтрофил содержит сегментированное на 2—5 долей ядро, уплотненный хроматин, а в цитоплазме — многочисленные мелкие секреторные гранулы трех типов. Часть гранул, дающих положительную окраску на фермент миелопероксидазу, представлена лизосомами, которые содержат лизоцим (повреждает стенку бактерий), низкомолекулярные катионные белки — дефенсины и кателицидины (нарушают дыхание и рост микроорганизмов и грибков; дефенсины повышают проницаемость сосудов микроциркуляторного русла), протеазы и кислые гидролазы — позволяют ней-трофилам легко переваривать фагоцитированные объекты. Гранулы 2-го типа содержат лактоферрин, обладающий бактериостатическим действием, транскобаламины I и III — переносчики витамина В12 в крови и лизоцим. Вещества гранул 3-го типа содержат кислые гликозаминогликаны, участвующие в процессах размножения, роста и регенерации тканей, благодаря их способности концентрировать факторы роста в тканях костного мозга. Гранулы 2-го и 3-го типов, содержащиеся в цитоплазме нейтрофилов, постоянно секретируют биологически активные вещества даже вне фагоцитоза. К ним относятся опухольнекротизирующий фактор а, интерлейкин-1, интерлейкин-6, интерлейкин-11. Вместе с такими же цитокинами, секре-тируемыми макрофагами в острой фазе заболевания, вызванного инфекцией, травмой (например, ожоговой), они стимулируют синтез и секрецию в кровь из печени так называемых белков острой фазы (с-реактивный белок, сц-антитрипсин, а,-кислый гликопротеин, церулоплазмин), повышающих устойчивость организма к инфекции, токсичным соединениям, образуемым микроорганизмами.
Нейтрофилы осуществляют свои функции благодаря способности быстро мигрировать и накапливаться в инфицированном или поврежденном участках организма, фагоцитировать, т. е. захватывать и разрушать в фагоцитарных вакуолях внутри клетки поглощенные бактерии и поврежденные клетки. Их способность к миграции связана с хорошо развитым аппаратом движения, выбор направления их движения к воспаленным или инфицированным тканям обусловлен появлением в этих тканях вазоактивных и хемотаксических факторов.
Вазоактивные факторы (дефенсины, гистамин, секретируемый под влиянием дефенсинов тучными клетками тканей) повышают проницаемость капилляров, что способствует миграции нейтрофилов в ткань. Хемотаксические факторы взаимодействуют с рецепторами на поверхности гранулоцитов, образуя лиганд-рецепторный комплекс, определяющий движение нейтрофилов к воспаленному участку. Мощным хе-мотаксическим эффектом обладают N-формилпепетиды бактериального происхождения и лейкотриены, производные метаболизма арахидоновой кислоты в мембране клеток. Лейкотриены секретируются активированными Т-лимфоцитами и макрофагами после воздействия на них бактериальных веществ. Помимо лейкотриенов эти клетки секретируют другие хемо-аттрактанты — эндотоксины. Важными хемотакическими факторами являются продукты активации комплемента — фрагменты его молекул С3в и С5а. Некоторые из этих факторов, особенно С3в, функционируют как опсонины, т. е. вещества, облегчающие фагоцитоз бактерий (от греческого орsonein — делать съедобным). Недостаточность хемотаксической активности нейтрофилов препятствует накоплению этих лейкоцитов в очаге воспаления, что способствует распространению инфекции в организме. К таким последствиям приводит, например, нарушение хемотаксиса нейтрофилов у больных при ожоговой болезни, диабете, при низком содержании белка в рационе человека.
Увеличение или уменьшение количества нейтрофилов в анализах
Данным кровяным клеткам свойственно также как бы ощущать «сигналы воспаления». Как только они их улавливают, они тут же перемещаются к воспалительным участкам. Это могут быть как травмы, так и раны, ожоги, язвы и так далее.
Снижение уровня данных клеток может отмечаться при наличии в организме определенных паразитарных заболеваний либо вирусов, а также на фоне приема тех или иных лекарственных препаратов.
Нейтрофилы – что это такое?
Процесс созревания нейтрофильных гранулоцитов происходит непосредственно в костном мозге, после чего они тут же проникают в кровь со скоростью примерно семь миллионов в минуту. В крови они остаются не более двух суток, после чего перемещаются в ткани и органы, защищая их от инфекционных патологий.
Самой главной функцией, возложенной на нейтрофилы, является уничтожение бактерий. В случае развития острой инфекционной патологии число данных кровяных клеток резко увеличивается. Следует отметить, что данные клетки могут выполнять свою функцию даже в тех тканях, которые получают очень маленькое количество кислорода. Это могут быть ткани, захваченные как отеком, так и воспалением.
Норма содержания нейтрофилов в крови
- В первый день в крови малыша содержится от одного до семнадцати процентов палочкоядерных нейтрофилов и от сорока пяти до восьмидесяти процентов сегментоядерных нейтрофилов.
- У детей в возрасте до двенадцати месяцев: пол – четыре процента палочкоядерных нейтрофилов и пятнадцать – сорок пять процентов сегментоядерных нейтрофилов.
- У детей в возрасте от одного года до двенадцати лет количество палочкоядерных нейтрофилов составляет пол – пять процентов, а сегментоядерных – двадцать пять – шестьдесят два процента.
- В возрасте от тринадцати до пятнадцати лет в крови ребенка насчитывается пол – шесть процентов палочкоядерных нейтрофилов и сорок – шестьдесят пять процентов сегментоядерных нейтрофилов.
Повышение уровня нейтрофилов в крови
Понижение уровня нейтрофилов в крови
Вернуться к началу страницы
Развитие нейтрофилов
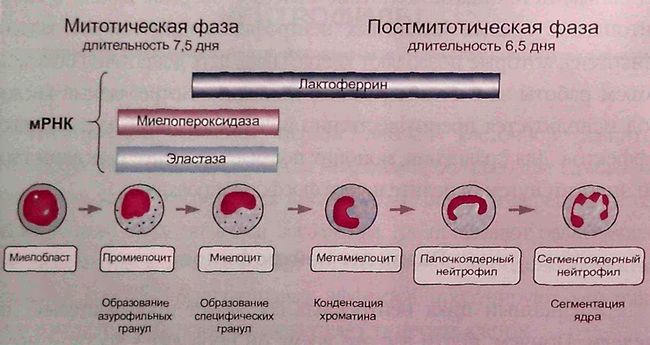
Жизненный цикл нейтрофила составляет приблизительно две недели. Причем, почти все это время он проводит в костном мозге. В его развитии выделяют две фазы:
- митотическую,
- постмитотическую.
Митотическая фаза
В митотическую фазу (ее продолжительность примерно 7,5 дня) клетка проходит несколько циклов деления. Сначала образуется миелобласт посредством дифференцировки стволовой клетки. Уже на следующей стадии (промиелоцит) формируются азурофильные гранулы, содержащие ферменты (миелопероксидазу, дефензины, эластазу). Эти гранулы еще называются «первичными», так как они образуются первыми. Позднее, на стадии миелоцита, появляются специфические гранулы, несущие лактоферрин и лизоцим. Они получили название вторичных. Разделение гранул на первичные и вторичные пришло из гистологии и с функциональных позиций довольно условно.
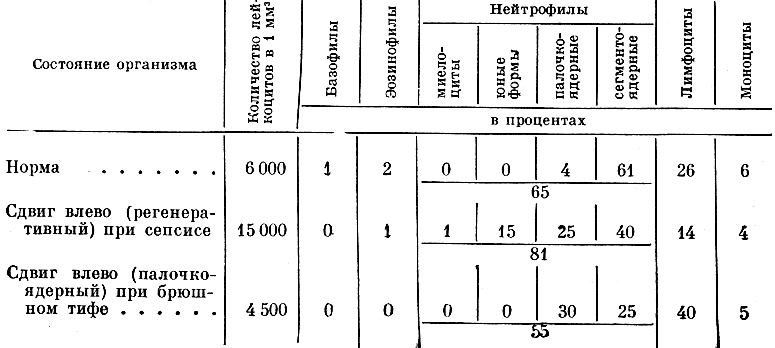
Норма
Лабораторные показатели нормы нейтрофилов у мужчин и женщин не зависят от пола обследуемого человека, а изменяются в зависимости от возраста.
В кровеносном русле одномоментно у человека присутствует несколько форм нейтрофильных клеток, различных по степени зрелости. У незрелых нейтрофилов ядро имеет вид палочки, ядро зрелых нейтрофилов разделено специальными перетяжками на несколько сегментов. Различие в строении ядра нейтрофилов обуславливает разделение их на палочко- и сегментоядерные.
Существует шесть форм зрелости нейтрофильных клеток, две из которых отмечаются в лабораторных анализах в здоровом организме, а остальные выявляются в случае развития тяжелого патологического процесса.
В бланках лабораторного исследования крови графа «нейтрофилы» отсутствует. В заключении выдается результат определения содержания незрелых и сегментоядерных клеток нейтрофилов. В здоровом организме количество незрелых нейтрофилов не превышает 12% у новорожденных, у всех остальных возрастных категорий данный показатель находится в пределах 1 – 5%. Максимальное количество сегментоядерных нейтрофилов характерно также для периода новорожденности (50 – 70%), с возрастом число зрелых клеток постепенно снижается и устанавливается в границах 40 – 60%.
У ребенка
Наиболее бурно изменяется содержание сегментоядерных нейтрофилов в крови у ребенка:
- у новорожденных – 50 – 70%;
- в течение первой недели жизни показатели снижаются до 35 – 55%;
- на второй неделе жизни границы нормы уменьшаются до 25 – 45%;
- 1 месяц – отмечается падение содержания данных клеток до 17 – 30%;
- 1 год – 45 – 65%;
- 5 лет – 35 – 55%;
- после 6 лет уровень содержания соответствует взрослой категории – 40 – 60%.
Максимальное число палочкоядерных нейтрофилов наблюдается у новорожденных – 5 – 12%. Уровень содержания незрелых нейтрофилов в детском организме остается практически неизменным после первой недели жизни – 1 – 5%.
Понижение
Если лабораторно установлено, что нейтрофилы понижены в крови, это говорит о развитии крайне тяжелых нарушений в организме и резкого ослабления его защитных механизмов.
Уменьшение числа нейтрофилов в крови (нейтропения) возможно в следующих случаях:
- крайне тяжелое протекание основного заболевания, в результате чего происходит гибель чрезмерного количества нейтрофилов. Подобную картину в анализах можно наблюдать при развитии таких острозаразных заболеваний, как тиф, туляремия. Также нейтропения наблюдается и при вирусном поражении организма, когда понижены лейкоциты в крови;
- нарушение процессов формирования новых нейтрофилов в костном мозге в результате уменьшения числа его структурных элементов. Поражение костного мозга может произойти в результате негативного воздействия некоторых лекарственных препаратов, ионизирующего излучения, проведения комплексного лечения раковых заболеваний (химиотерапия, усиленная методами лучевой терапии);
- прогрессирование онкологических заболеваний крови.
При тяжелых заболеваниях, уровень нейтрофилов сильно снижается
Как и в случае нейтрофилии, различают три степени нейтропении:
- мягкая – снижение уровня нейтрофилов до 1*109/л;
- умеренная – уменьшение концентрации до 0,5*109/л;
- тяжелая – содержание клеток меньше 0,5*109/л.
Причины снижения уровня содержания нейтрофилов в крови могут быть обусловлены физиологическими процессами, как и при нейтропении.
Согласно многочисленным исследованиям было установлено, что до 25% населения земного шара имеют постоянный сниженный уровень нейтрофилов. При этом у этих людей отсутствуют какие-либо жалобы на здоровье и в лабораторных результатах исследования их крови все остальные показатели находятся в пределах нормы.
Также известны случаи зависимости содержания нейтрофилов в крови от индивидуальных биологических ритмов. У некоторых людей периодически отмечается полное исчезновение этих форм клеток с одномоментным возрастанием количества других видов лейкоцитов – моноцитов и эозинофилов крови. При этом отсутствует патологическая симптоматика. Через некоторое время показатели лабораторного обследования приходят в норму самостоятельно, без специализированного вмешательства.
Еще одной физиологической причиной снижения нейтрофильных клеток в организме является генетическое заболевание – нейтропения Костмана, которая характеризуется полным отсутствием нейтрофилов. Дети с этим диагнозом в течение первого года жизни подвержены высокому риску генерализации малейшего инфекционного процесса, но если ребенок выживает в течение этого периода, в последующем отсутствие нейтрофилов компенсируется организмом за счет повышения моноцитов и эозинофилов. При этом складываются довольно положительные прогнозы данного заболевания, ребенок может прожить много лет.
Распознавание чужеродных объектов
опсонинами
Опсонины
Опсонины — собственные продукты макроорганизма, выступающие в роли посредников между рецепторами на поверхности мембран фагоцитирующих клеток и структурами бактерий, располагаемыми на поверхности. Фагоцитами они распознаются только после их адсорбции на микробной клетке.
Наиболее важными опсонинами являются инактивированный компонент комплемента іСЗb и антитела класса G. Притом на начальной стадии инфекционного процесса, когда уровень антимикробных антител довольно низкий, главную роль в опсонизации играет iСЗb. Нейтрофил имеет три типа рецепторов к комплементу:
- CR1,
- CR3,
- CR4.
CR3 и CR4 (β2-интегрины) обладают способностью связывать фиксированный на бактериальной клетке iСЗb. CR1 — вспомогательный рецептор, необходимый в ситуациях, когда СЗb на микробной мембране не инактивирован. Взаимодействие CR1-СЗb приводит к инактивации СЗb под действием фактора I комплемента. В реализации процесса поглощения для нейтрофилов наиболее важен CR3; у моноцитов и макрофагов приоритетное значение имеет CR4.
Распознавание нейтрофилом объекта при посредничестве антител класса G происходит за счет Fcγ-рецептора (FcγR). Fcγ-рецептор связывается с Fc-фрагментом антитела, вступившего во взаимодействие с антигеном (но не свободной молекулой).
Известно три разновидности Fcγ-рецепторов:
- FcγRI (CD64),
- FcγRII (CD32),
- FcγRIII (CD16).
FcγRI — высокоаффинный рецептор, присутствующий на макрофагах. Связывающая активность FcγRII и FcγRIII существенно ниже. Они обнаружены на нейтрофилах и макрофагах. Рецепторы для антител класса M на фагоцитах отсутствуют, однако имеются рецепторы для иммуноглобулинов класса А.
В роли опсонинов могут выступать и другие белки, например, LPS-связывающий протеин и септин. Оба они способны непосредственно взаимодействовать с наружной мембраной грамотрицательных бактерий, оба затем связываются с CD14 на поверхности фагоцита. Плотность CD14 высока на макрофагах; нейтрофилы начинают экспрессировать этот рецептор после активации такими медиаторами. как TNF-α, колониестимулирующие факторы и N-формил-метионил пептиды.
Еще один опсонин — С-реактивный белок (СРБ). Его концентрация в крови в период воспаления может увеличиваться в сотни и тысячи раз. Этот белок имеет сайты связывания для C-полисахарида пневмококка, фосфолипидов мембран, ДНК. Рецептор для СРБ на нейтрофилах отсутствует. Опсонизация происходит опосредованно — через активацию системы комплемента по классическому пути. Значение СРБ велико при воспалительных процессах неинфекционной этиологии. Будучи способным связываться с эндогенными структурами (поврежденными мембранами, ДНК, фибрином), он выступает в качестве основного опсонина стерильных очагов тканевой деструкции (инфаркт миокарда, закрытые травмы).
Заключение
Являясь самой многочисленной группой клеток среди всех видов форменных элементов крови, нейтрофилы играют огромную роль в диагностическом процессе. Любое отклонение показателей нейтрофилов в крови требуют проведения дополнительного обследования с целью установления истинной причины нарушения. В некоторых случаях изменение количества нейтрофилов может быть обусловлено физиологическими процессами и не вызывать никаких опасений. Однако, зачастую изменение концентрации данного типа клеток является первым признаком развития крайне тяжелых состояний, требующих серьезного подхода для их устранения.
Своевременное установление провоцирующих факторов и вовремя предпринятые меры для устранения их действия поможет избежать развития осложнений. Так, если снижение уровня нейтрофилов вызвано развитием в организме дисбаланса питательных веществ, вовремя проведенная коррекция данного состояния (назначение курса витаминотерапии или специально подобранная диета) быстро приведет показатели содержания нейтрофилов к норме.
Если количественные изменения нейтрофилов произошли на фоне приема некоторых лекарственных препаратов, как одно из побочных эффектов их действия, врач пересмотрит разработанную тактику лечения и подберет другие фармацевтические средства.
Специфических лечебных мероприятий, направленных непосредственно на коррекцию содержания в крови нейтрофилов, в современной медицине не существует. Для того, чтобы привести данный показатель в пределы нормы нейтрофилов, необходимо устранить действие провоцирующего фактора, ликвидировать заболевание, спровоцировавшее изменение лабораторных показателей крови.
После выздоровления от основного заболевания уровень содержания нейтрофилов, как правило, приходит в норму самостоятельно.