Лечение
Специфического лечения миопатии Дюшенна не существует. Терапия заключается лишь в симптоматических мерах, направленных на замедление патологического процесса. Пациентам назначают:
- анаболические стероиды, аденозинтрифосфат и актопротекторы для активизации процессов метаболизма в мышечной ткани;
- медпрепараты для облегчения передачи нервно-мышечного сокращения;
- массаж, лечебную физкультуру (ЛФК) и другие физиотерапевтические процедуры, позволяющие снизить контрактуру мышц, избежать дисфункциональной атрофии.
Чтобы временно сохранить способность стоять и передвигаться, а также предотвратить сгибательные контрактуры, пациентам с дистрофией Дюшенна показаны специальные ортопедические приспособления (ортезы, бандажи, корсеты и т.д.). При тяжелых поражениях костной системы требуется хирургическая коррекция. В случае снижения жизненной емкости легких более 35 % во время сна подключают аппарат ИВЛ. Иногда для поддержания функции дыхания ребенку необходима трахеостомия.
Специалисты-генетики, биохимики и неврологи сегодня усиленно работают над поиском эффективных методов лечения дистрофии Дюшенна. Стоит отметить несколько перспективных разработок: экзон-скиппинг, позволяющий корректировать мутации, а также технологию продуцирования Дт-подобного белка утрофина и пересадку стволовых клеток.
Диагностические мероприятия
Диагностика синдрома Дюшенна не вызывает трудностей у специалистов, поскольку имеет весьма специфические симптомы.
Врачи традиционно начинают с опроса больного или его родителей и сбора анамнестических данных
Особое внимание они уделяют:
- Времени появления первых симптомов,
- Локализации первичной мышечной слабости,
- Общему самочувствию пациента,
- Наличию подобных расстройств у родных и близких.
Во время неврологического обследования выявляется:
- Слабость определенной группы мышц и определяется ее степень,
- Изменение мышечного тонуса,
- Атрофические процессы,
- Гипо- и арефлексия,
- Деформация стопы, груди, позвоночного столба.
Врачи наблюдают за больным ребенком, обращая внимание на то, как он ходит, бегает и встает с пола. Изменение походки — важный диагностический признак миопатии
После проведения первичных диагностических процедур врачи могут заподозрить наличие у больного патологии и поставить предварительный диагноз. Чтобы его подтвердить или опровергнуть, пациента направляют на лабораторно-инструментальное обследование.
- Анализ крови на гормональный статус.
- Биохимический анализ крови на активность креатинкиназы – фермента, уровень которого у больных детей очень высок. Если КФК в норме, миопатию Дюшена исключают.
- Иммуногистохимическое исследование – микроскопия биоптата мышечной ткани, взятого от больного, с целью определения белка дистрофина. У лиц с миопатией он отсутствует.
- ДНК-тест – генетическое исследование крови больного, позволяющее определить мутантный ген и точно диагностировать патологию.
Дополнительные диагностические методики:
- Электрокардиография — выявление признаков поражения миокарда.
- Электромиография — определение фибрилляции, свидетельствующей о некрозе мышечных волокон. Эта методика оценивает состояние скелетной мускулатуры и подтверждает, что в основе патологии лежит именно поражение мышц, а не нарушение передачи нервных импульсов.
- Дыхательные пробы, рентгенография позвоночника и органов грудной клетки, УЗИ сердца — методы, не оказывающие существенного влияния на процесс постановки диагноза, но позволяющие выявить имеющиеся отклонения в структуре и функционировании органов дыхания и сердца.
Симптомы
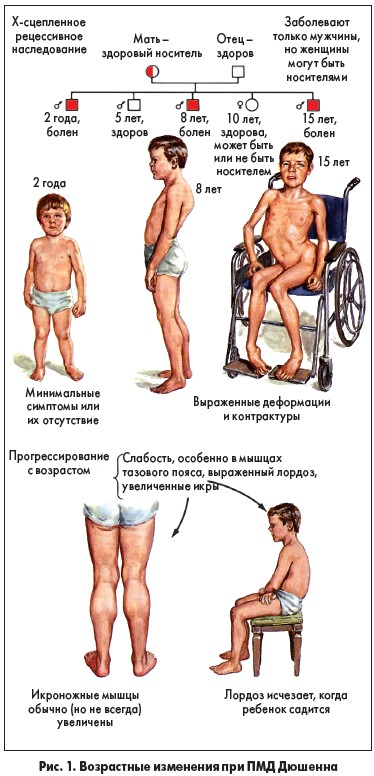
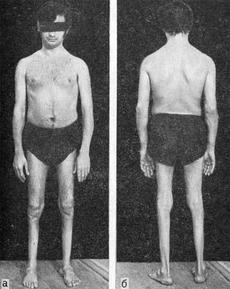
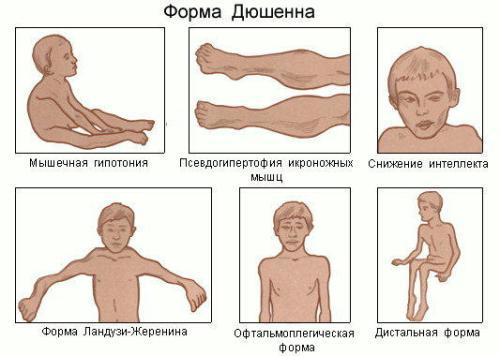
Первые признаки прогрессирующей миопатии Дюшена появляются в возрасте от года до пяти лет. В большинстве случаев уже в первые 12 месяцев наблюдается несколько замедленное развитие двигательных функций ребенка. Он позже начинает садиться, вставать и ходить. При хождении малыш часто падает и спотыкается.
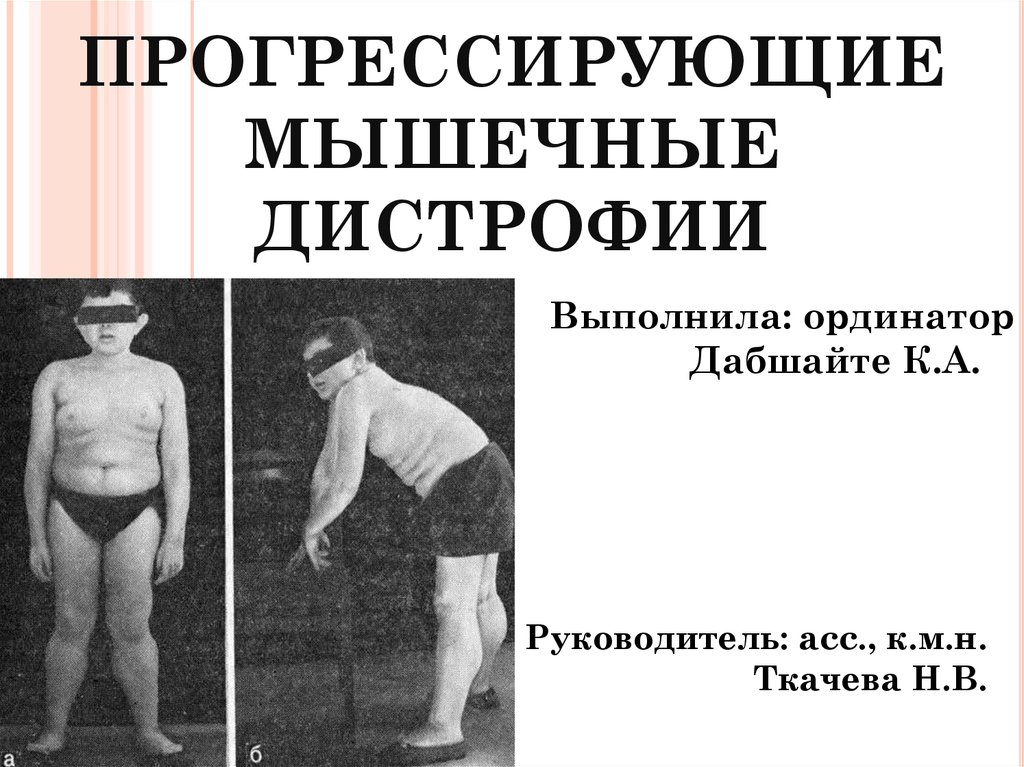
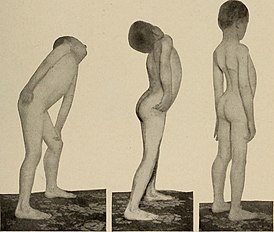
Через год или два слабость мышц становится более выраженной: ребенку трудно подниматься по лестничным ступеням, долго находиться на ногах и вставать с колен. У детей с мышечной дистрофией вырабатывается характерная «утиная» походка: они ходят, переваливаясь с ноги на ногу, как утки.
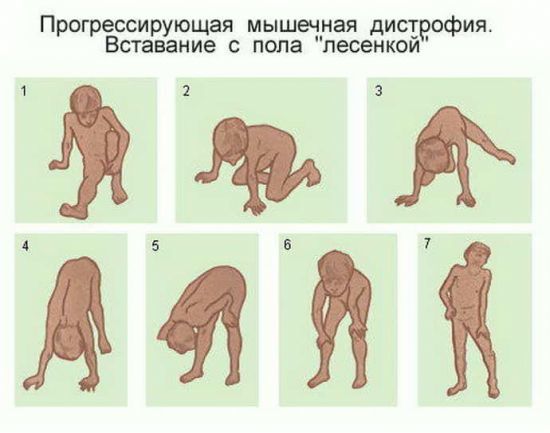
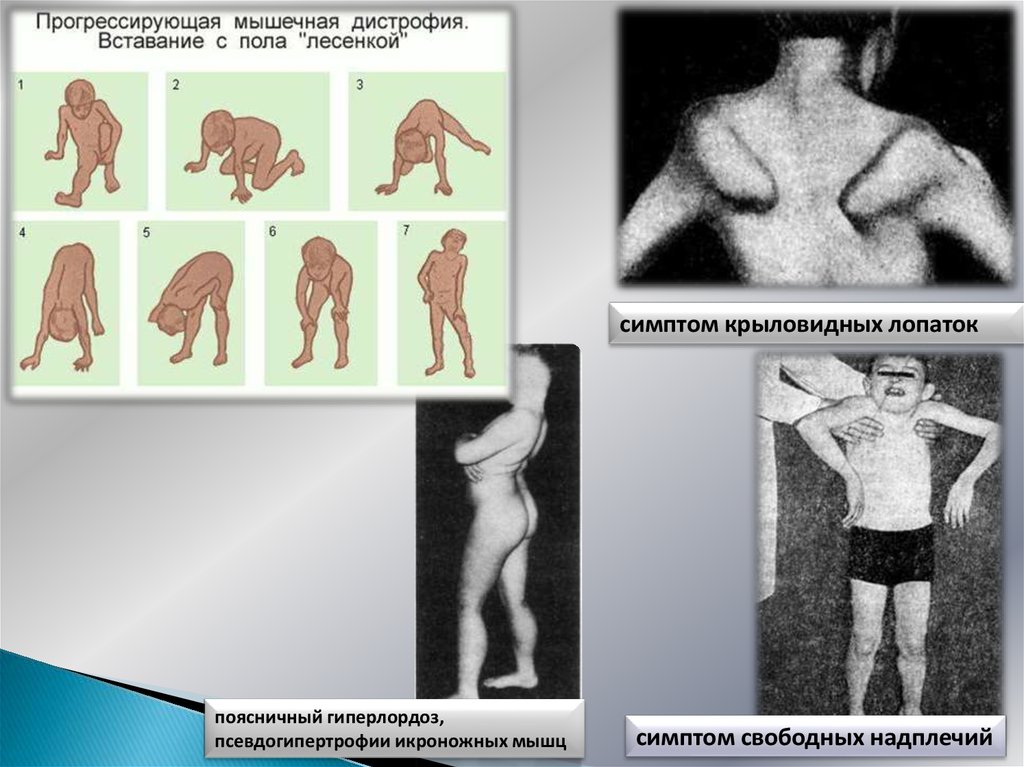
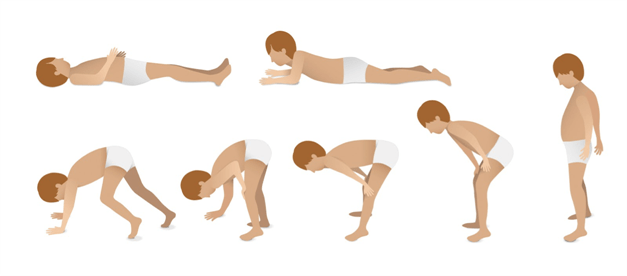
ФАКТ! Когда ребенок пытается встать из положения сидя на корточках, он инстинктивно опирается на бедра и талию, как бы взбираясь по собственному телу вверх.
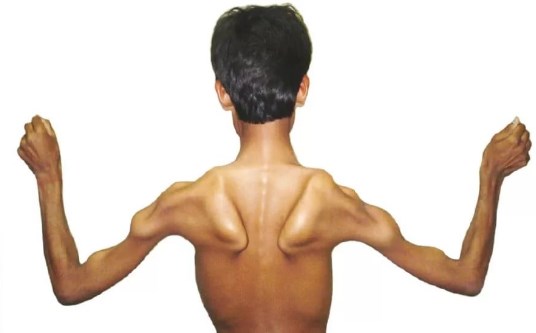
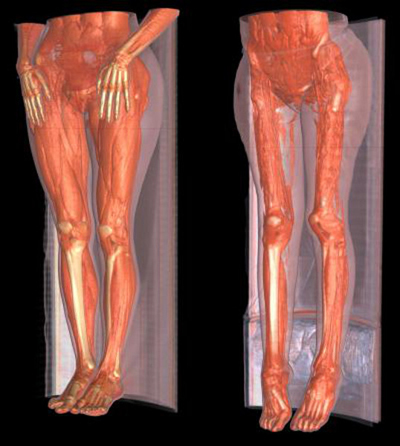
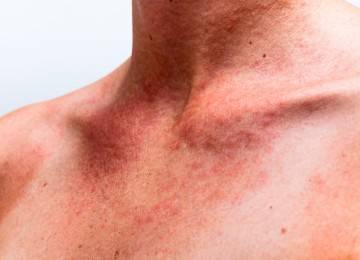
Амиотрофия Дюшена стартует с тазовых мышц и постепенно распространяется на грудь, верхнюю часть спины, плечи и руки. Пораженные мышцы уменьшаются в объеме, атрофируются, из-за чего талия становится тонкой, и сильно выступают лопатки.
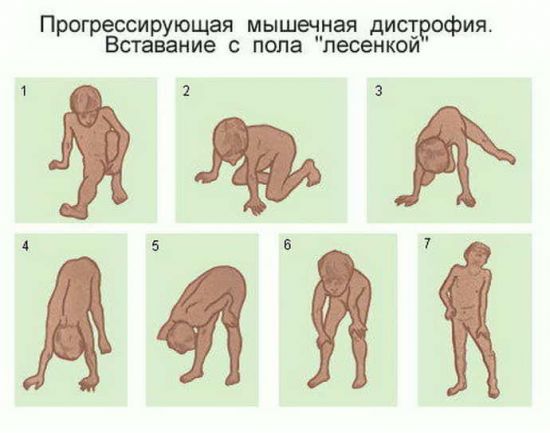
Типичный признак миопатии – гипертрофированные, как будто перекачанные, икроножные мышцы. Снижаются и выпадают сухожильные рефлексы: вначале коленные, затем с бицепса и трицепса. Дольше всего сохраняются пястно-лучевые и ахилловы рефлексы.
Парез Дюшена-Эрба
Клиническая картина миопатии может включать следующие симптомы:
- искривление позвоночника в передне-заднем или боковом направлении;
- килевидную или седловидную деформацию грудной клетки;
- искажение формы стоп;
- аритмию, перепады артериального давления, нарушение сердечной деятельности;
- избыточный вес и недоразвитие половых желез (синдром Пехкранца-Бабинского-Фрелиха);
- ожирение на фоне развития синдрома Иценко-Кушинга;
- олигофрению, чаще в стадии дебильности (в 30% случаев);
- повышенную возбудимость;
- ухудшение речевой функции и кратковременной памяти;
- аутизм.
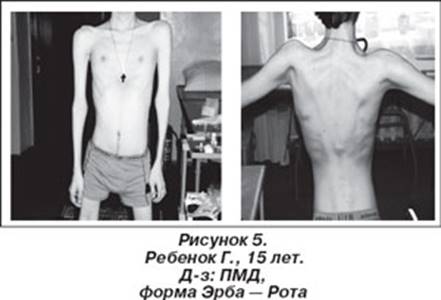
Всего за 4-5 лет миопатия Дюшена приводит к значительному ограничению двигательной способности. К началу пубертатного периода дети уже не могут ходить, а к 15 годам не в состоянии совершать даже простые движения.
Поскольку патологический процесс захватывает дыхательную мускулатуру, жизненная емкость легких стремительно снижается. Дышать самостоятельно становится все труднее, а затем и вовсе невозможно.
Признаки и симптомы мышечной дистрофии Дюшенна
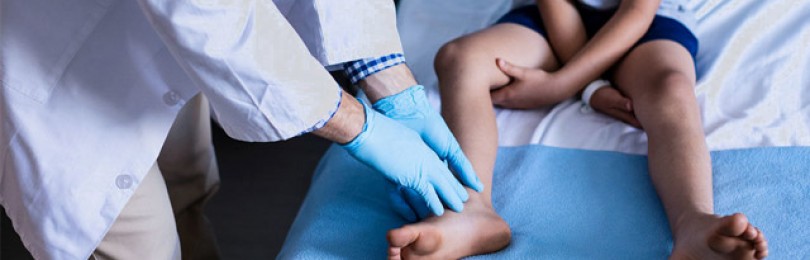
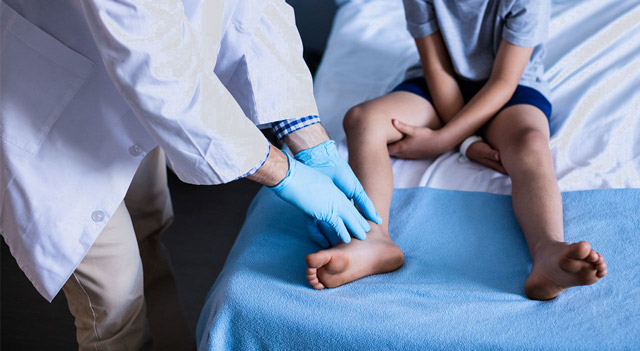
Дети с мышечной дистрофией Дюшенна (МДД) часто поздно начинают ходить.
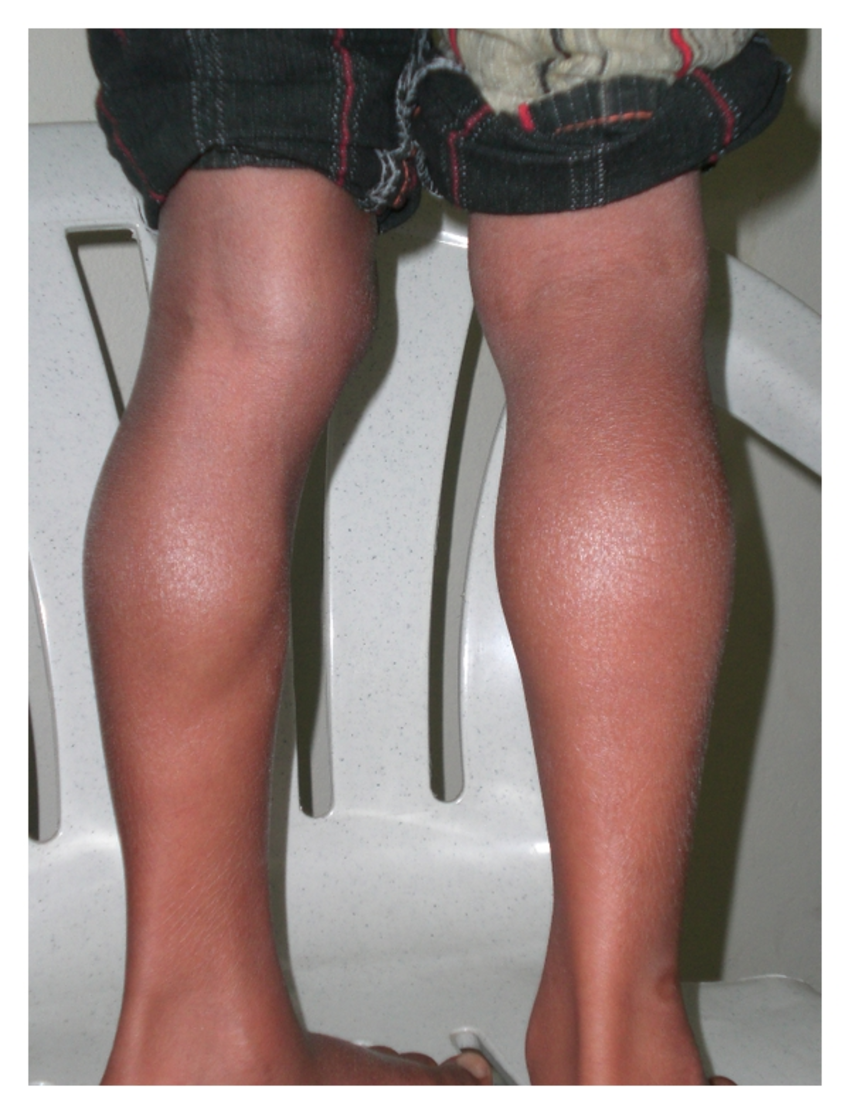
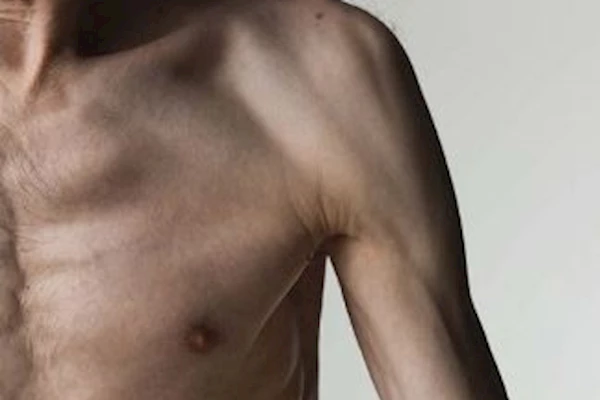
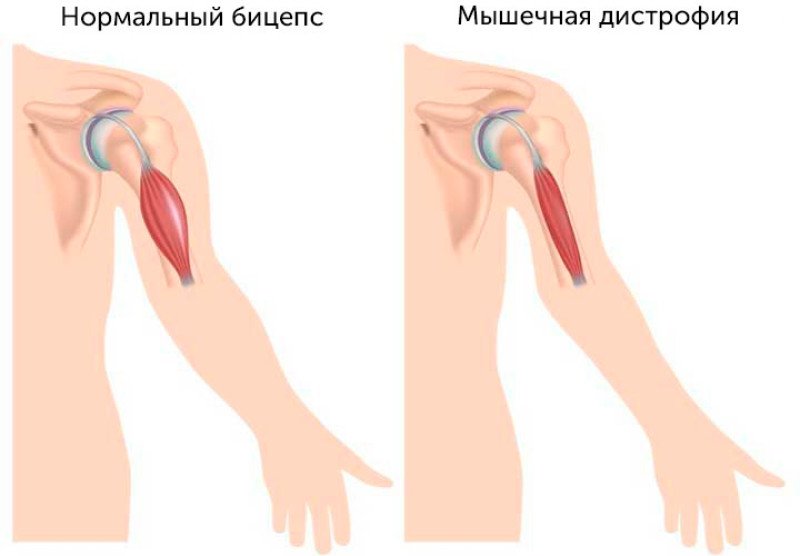
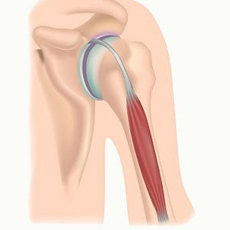
У малышей родители могут заметить увеличение икроножных мышц (см. изображение справа). Это увеличение известно как псевдогипертрофия, или «ложное увеличение» мышц, потому что мышечная ткань является ненормальной и может содержать рубцовую ткань.
Дошкольник с МДД может показаться неуклюжим и часто падать. Родители также могут заметить, что детям трудно подниматься по лестнице, вставать с постели или бегать.
К школьному возрасту детям тяжело ходить и передвигаться, ребенок часто падает. Чтобы сохранить равновесие, они могут выпячивать животы и откидывать плечи. Детям также трудно поднимать руки.
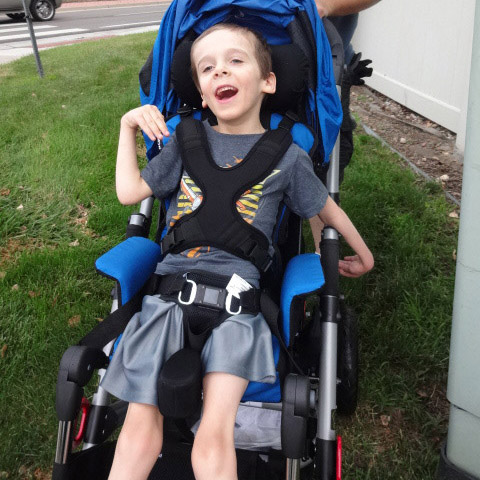
Многие дети с МДД начинают пользоваться инвалидной коляской в возрасте от 7 до 12 лет. Переход на инвалидную коляску обычно происходит постепенно; сначала кресло может потребоваться только для сохранения энергии ребенка при преодолении больших расстояний. (Дети часто вырабатывают новую самостоятельность после полного перехода на инвалидную коляску с электроприводом.)
В подростковом возрасте для действий, связанных с руками, ногами или туловищем, может потребоваться помощь или механическая поддержка.
Боль и чувствительность
Мышечная дистрофия Дюшенна само по себе обычно не болезненна. Некоторые люди иногда сообщают о мышечных судорогах; обычно их можно лечить безрецептурными болеутоляющими средствами.
Поскольку мышечная дистрофия не влияет непосредственно на нервы, осязание и другие чувства остаются нормальными, как и контроль над гладкими или непроизвольными мышцами мочевого пузыря, кишечника и половыми функциями.
Сердце
Недостаток дистрофина может ослабить мышечный слой сердца (миокард), что приводит к состоянию, которое называется кардиомиопатией. Со временем, иногда еще в подростковом возрасте, ущерб, нанесенный МДД сердцу, может стать опасным для жизни. Сердце должно тщательно и постоянно контролироваться, как правило, детским кардиологом.
Дыхательная функция
Начиная примерно с 10-летнего возраста, диафрагма и другие мышцы, управляющие легкими, могут ослабнуть, что сделает легкие менее эффективными при движении воздуха внутрь и наружу. Хотя ребенок может не жаловаться на одышку, к числу проблем и признаков, указывающих на плохое состояние дыхания, относятся головные боли, умственная отсталость, трудности с концентрацией или бессонницей, а также ночные кошмары.
Ослабленные дыхательные мышцы затрудняют кашель, что приводит к повышенному риску серьезной респираторной инфекции. Простая простуда может быстро перерасти в пневмонию
Важно сделать прививку от гриппа, а при возникновении инфекции — получить быстрое лечение
Неспособностью к обучению
Около треть мальчиков с МДД имеют некоторую степень неспособности к обучению, хотя немногие имеют серьезную умственную отсталость.
Врачи считают, что аномалии дистрофина в мозге могут оказывать незначительное влияние на когнитивные функции и поведение. Проблемы с обучением при МДД возникают в трех основных областях:
- концентрация внимания;
- словесное обучение и память;
- эмоциональное взаимодействие.
Дети с подозрением на нарушение способности к обучению могут быть обследованы психоневрологом-воспитателем или педиатром.
Если диагностирована неспособность к обучению, образовательные и психологические вмешательства могут начаться сразу же. Специалист может назначить упражнения и методы, которые могут помочь улучшить эти области, а специализированные школы могут оказать особую помощь в обучении.
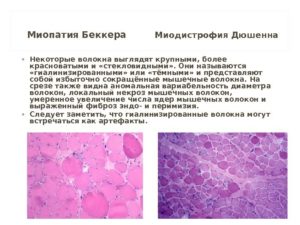
Мышечная дистрофия Беккера – восстановления силы в мышцах при миодистрофии
По локализации болиМышечная дистрофия Беккера
Сергею 19 лет. Диагноз: мышечная дистрофия Беккера.
Мышечная дистрофия у Сергея начала проявляться в возрасте 10 лет. Заболевание началось с общей физической слабости. Особенно слабость проявлялась на уроках физкультуры. Затем Сергей стал замечать, что он садится на корточки не так, как его одноклассники. садились мягко, а Сергей падал на корточки и придерживался рукой, чтобы не упасть. Встать без помощи рук мальчик не мог.
Молодой человек стал замечать, что слабость симметричная в обеих ногах. Родители Сергея, когда обращались к врачам по поводу слабости сына, отмечали, что икроножные мышцы очень плотные и объемные, очень похожи на бутылки. Это состояние икроножных мышц называется псевдогипертрофией.
У Сергея стал проявляться прогрессирующий поясничный лордоз, который прогрессировал с годами все сильнее и сильнее, появилась “ утиная” походка.
При подъеме с пола, Сергей вставал, подтягиваясь на руках. Он перестал бегать, так как все время спотыкался, и мышечная слабость так сильно усиливалась, что бег приходилось прекращать через несколько шагов.
Вот с такими проблемами обратился ко мне, Никонову Николаю Борисовичу, Сергей, с просьбой научить его родителей воздействовать на мышцы так, чтобы они стали работать лучше.
Доктор Никонов
Сергей и его родители знали о том, что полное обездвиживание может наступить уже в 25 лет.
Так было с одной моей пациенткой, которая обратилась ко мне в 60 лет в полуподвижном состоянии.
После проведения процедур по моей методике, Эмине, так зовут пациентку, стала свободно подниматься с пола без помощи рук, и, подниматься довольно быстро по лестнице на 17 этаж без помощи рук и без перерыва на отдых. Подробнее о восстановлении Эмине смотрите на видео:
У Сергея была повышенная концентрация креатинфосфокиназы в сыворотке крови и миоглобинурия. Так как отличить миодистрофию Беккера от миодистрофии Дюшенна трудно, то сохранение силы сгибательных мышц шеи позволяет дифференцировать диагнозы.
У Сергея сохранились силы сгибательных мышц шеи – у него мышечная дистрофия Беккера, а у Эмине, Насти и Якоба, моих пациентов, мышцы шеи были бессильны.
Мышечная дистрофия Беккера образуется в результате того, что ген, вырабатывающий белок дистрофин, поврежден. Дистрофин вырабатывается, но в других конфигурациях. Белок дистрофин – самый большой белок в мышечной клетке. Он делает каркас для клетки, чтобы она была полая внутри. Каркас мышечной клетки состоит из белка дистрофина и напоминает металлическую сетку с дырками.
Через эти дырки внутрь клетки попадают питательные вещества и выходят отработанные шлаки. Так как сетка дистрофина не целиковая, как кирпичная стена, то эта сетка может расширяться и сужаться. Расширяют и сужают сетку два двигательных белка внутри этого каркаса – актин и миозин. Актин и миозин могут двигаться, если им дать энергию.
Энергию двигательным белкам дает митохондрия.
Доктор Никонов
Когда я посмотрел на строение мышечной клетки при миодистрофии Беккера в электронный микроскоп, то увидел, что внутри мышечной клетки митохондрии располагаются не у двигательных белков, а на периферии клетки. Так же я увидел, что внутри мышечной клетки много жировых включений. Значит, что эти жировые включения отодвинули митохондрии от их рабочих мест и двигательные белки работать не могут.
Так выглядят мышцы при мышечной дистрофии Беккера под электронным микроскопом
A: Нормальная мышца здорового человека.
B: Гипертрофированная мышца при мышечной дистрофии Беккера.
Доктор Никонов
В результате воздействия на мышцы моим методом, у Сергея стала появляться Сила в мышцах. Он стал ходить уверенно с опущенными вниз руками, стал ходить на полную стопу, стал передвигаться в пространстве так, как обычный человек.
Начало процедур по восстановлению движения мышц Сергея
Самое сложное – это начало процедур. На первых занятиях с Сергеем принимали участие: я, родители Сергея, моя жена Никонова Лилия Александровна, наш сын Степан (10 лет) и сестра Сергея (10 лет). Младшие наши помощники отвечали за фиксацию ног Сергея. Задача для них обоих была выполнимая.
Процесс восстановления Сергея
Доктор Никонов
В этой статье я выражаю Благодарность моей жене Никоновой Лилии Александровне и моим маленьким помощникам, которые, по Доброй Воле, помогали мне восстанавливать движения мышц Сергея.
Миодистрофия Беккера. Никонов Николай Борисович, Никонова Лилия Александровна, Сергей с родителями и сестрой после проведения консультаций процедур.
Мышечная дистрофия Беккера. Никонов Николай Борисович с Сергеем
Обучение родителей самим восстанавливать силу в мышцах.
Прогрессирование поясно-конечностной мышечной дистрофии
На настоящий момент прогрессирование каждого типа ПКМД не может быть предсказано точно, однако информация о генетической мутации, спровоцировавшей развитие ПКМД, может помочь. Некоторые формы ПКМД прогрессируют быстро (потеря способности ходить может произойти в течение небольшого количества лет) и влекут серьёзную степень обездвиженности. В то время как другие формы ПКМД прогрессируют медленно, причиняя минимальный вред двигательной способности.
ПКМД может стартовать в детстве, юношестве, раннем взрослом периоде или даже позже. Развитие ПКМД не зависит от пола человека.
Некоторые врачи приходят к выводу, что если ПКМД начинается в детстве, то прогрессирование обычно происходит быстрее, приводя к бОльшей степени инвалидности. Если же ПКМД начинается в юношестве или зрелом возрасте, то заболевание протекает в более слабой форме и прогрессирует медленнее.
Основные причины
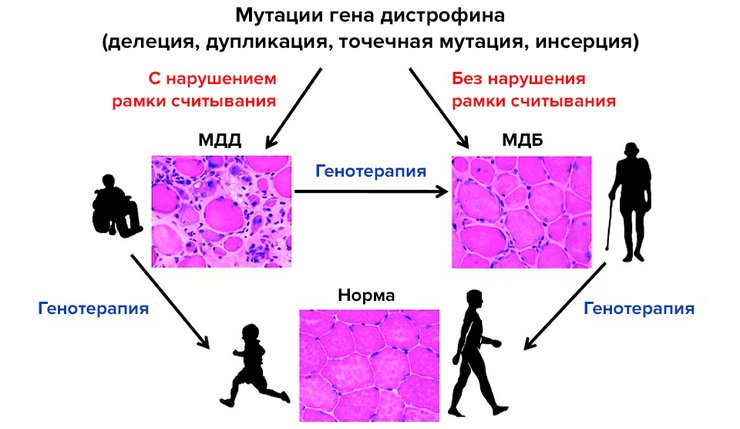
Мышечная дистрофия является следствием отклонения в генетическом коде ДНК. Мутация возникает в расположенном в Х-хромосоме гене. Один из его участков отвечает за выработку особого белка — дистрофина. Это вещество на микроскопическом уровне составляет базис мышечных волокон и выполняет несколько функций:
- поддержание клеточного скелета;
- обеспечение способности мышечных волокон к сокращению и расслаблению.
При этом заболевании дистрофин отсутствует или плохо синтезируется. Уровень «нормального» белка не превышает отметки в 3 %. Такая мутация приводит к разрушению волокон в мышцах. Они постепенно перерождаются, замещаются жировой и соединительной тканью. Как следствие, человек утрачивает способность к передвижению.
Какой имеет мышечная дистрофия Дюшенна тип наследования? Заболевание передается по рецессивному признаку. В организме человека все гены парные. Чтобы при наследственном недуге появились патологические нарушения, генетический дефект должен возникнуть в одной хромосоме или в аналогичных участках обеих. Во втором случае речь идет о рецессивном типе наследования.
Если генетический дефект диагностируется только в одной хромосоме, но болезнь при этом прогрессирует, говорят о доминантном признаке передачи. Рецессивный тип возможен при одномоментном поражении одинаковых ДНК-структур. Когда вторая хромосома абсолютно «здорова», патология не развивается. Поэтому дистрофия диагностируется только у лиц мужского пола. У них в генетическом наборе присутствует одна Х-хромосома, а вторая (У) — парная.
Что наука говорит о представительницах прекрасного пола? Мышечная дистрофия Дюшенна у девочек диагностируется редко. Для этого в генотипе должны совпасть две патологические Х-хромосомы, что маловероятно. Девочки могут выступать только носителями недуга и передавать его сыновьям.
Профилактика и прогноз
Супругам, в роду которых имелись случаи наследственных заболеваний, перед планированием беременности необходимо посетить врача-генетика. Профилактика патологии также заключается в проведении пренатальной диагностики. Выявив миопатию на ранних сроках, можно прервать беременность.
Миопатия Дюшена — наследственная патология, отличающаяся тяжелым течением и быстрым прогрессированием. Это современная медицинская проблема, характеризующаяся разрушением мышечной ткани и быстрым развитием мышечной слабости. Все без исключения больные погибают в раннем возрасте из-за развития не совместимых с жизнью осложнений. Только адекватная и комплексная терапия, четкое соблюдение рекомендаций врача, тщательный уход и забота родителей могут замедлить ход болезни.
Больные быстро становятся инвалидами и погибают в совсем юные годы. Самое страшное, что детям с миопатией не в силах помочь даже квалифицированные врачи, современные медицинские технологии и терапевтические методики 21 века. Болезнь до сих пор остается неизлечимой, забирая молодые жизни. Современные ученые-медики всего мира трудятся над созданием радикального способа борьбы с миопатией Дюшенна.
Диагностика миопатии Дюшена в Германии
Миопатия Дюшенна имеет свои диагностические признаки. Во-первых, это ЭКГ-исследование, во время которого выявляются поражения миокарда, стенок левого желудочка. Во-вторых, это повышенное содержание уровня дистрофина в ткани мышц. Однако дистрофия мышц при миопатии Дюшена не выявляется. В-третьих, это анализ крови, в котором можно определить активность фермента креатинфосфокиназы. При анализе у представительниц женского пола, которые являются носителями этого заболевания, этот фермент также повышен.
При тяжёлом течении и быстром прогрессировании лечение заболевания чаще всего не даёт никакого эффекта. Поэтому основная терапия носит симптоматический характер. Чаще всего в лечении используют витамины групп В и Е, аминокислоты, препараты кальция, анаболики, калия оротат, прозерин, галантамин, оксазилом.
Кроме того, применяют лечебную физкультуру, электрофорез с прозерином, ванны, индуктотерапию. Курсы повторяют каждые 2 месяца. Если же ребёнок неподвижен, то лечение проводится только в домашних условиях.
В жизни пациента с миопатией Дюшена большое значение имеет правильное питание. Нужно исключить чай и кофе, пряности и сладости, картофель и капусту. В рацион должны непременно входить овощи, фрукты, кисломолочные продукты, крупы, яйца, орехи и мёд.
Что же касается профилактики заболевания, то сделать это сложно, так как заболевание носит генетический характер. Обнаружить заболевание у плода до его рождения практически невозможно.
Восстановление коленных и тазобедренных суставов при артрозе — бесплатная видеозапись вебинара, который проводил врач ЛФК и спортивной медицины — Александра Бонина
Бесплатные уроки по лечению болей в пояснице от дипломированного врача ЛФК. Этот врач разработал уникальную систему восстановления всех отделов позвоночника и помог уже более 2000 клиентам с различными проблемами со спиной и шеей!
Хотите узнать, как лечить защемление седалищного нерва? Тогда внимательно посмотрите видео по этой ссылке .
10 необходимых компонентов питания для здорового позвоночника — в этом отчете вы узнаете, каким должен быть ежедневный рацион, чтобы вы и ваш позвоночник всегда были в здоровом теле и духе. Очень полезная информация!

УЗИ брюшной полости
Тактика терапии заболевания
Начинать лечение мышечной дистрофии нужно с устранения опасных симптомов, так как для решения генетических проблем актуальных методов коррекции пока что не существует. Например, при повреждении позвоночных мышц назначают препараты, улучшающие тонус.
Большая часть препаратов относится к группе сильнодействующих средств и назначается врачом строго по рецепту. Кроме лекарств, врачи рекомендуют использовать ортопедические аппараты для укрепления мышц и кистей. Для укрепления мышечной ткани также используют анаболические стероиды.
Генная терапия – сложный и ненадежный метод лечения, однако она быстро развивается. Например, для лечения синдрома Дюшена используют искусственно созданный ген, который затем вживляют человеку. Для этого внутрь аденовируса помещают нужный ген и вводят в мышечную ткань.
Что такое миопатия Дюшенна?
Миопатия Дюшена – это одно из самых грозных заболеваний среди всех первичных мышечных дистрофий. Начинается она в раннем детстве и заканчиваетсят летальным исходом ещё до того, как человеку исполнится 25 лет. Полное название болезни — прогрессирующая мышечная дистрофия Дюшена.

осмотр ребенка у врача
После поступления пациентов в немецкие клиники специалисты проводят опрос их жалоб, анамнеза заболевания и жизни, а также общий осмотр
Для лечащего врача очень важно выявить генетическую предрасположенность у пациента к миопатии Дюшена. Поэтому очень часто ребенка обследуют вместе с мамой (которая является носителем патологического гена)
В обязательном порядке больному ребенку назначаются консультации кардиолога, ортопеда и невролога.
Для подтверждения основного диагноза используются следующие лабораторные и инструментальные методы исследований:
- Развернутый анализ крови;
- Общий анализ мочи;
- Биохимическое исследование крови с обязательным определением концентрации общего билирубина и его фракций, мочевины, мочевой кислоты, креатинина, общего белка. Особым значением в диагностике миопатии Дюшена является повышение концентрации креатинфосфокиназы (специфический фермент, который повышается при повреждении мышечной ткани). КФК повышается не только у больного ребенка, но и его у мамы;
- Рентгенологическое исследование органов грудной полости;
- УЗИ органов брюшной полости и забрюшинного пространства;
- ЭКГ – отмечается гипертрофия левого желудочка и различные нарушения ритма сердца;
- Определение концентрации дистрофина в мышечной ткани;
- Биопсия мышц с последующим гистологическим исследованием биоптата. При этом специалист должен проводить исследование только на наименее поврежденных мышцах, в противном случае исследование будет неинформативным;
- Электромиография;
- Консультация генетика с кариотипированием.

УЗИ брюшной полости
Причины дистрофии Дюшена
Патология появляется вследствие генной мутации, имеющей место в области хр21. Более четверти таких патологий связывают со стойким изменением генотипа в материнской яйцеклетке. Остальные случаи объясняют гетерозиготностью мамы пациента по патологии мутагенеза в гене дистрофина.
Принято считать, что примерно 7% всех периодически возникающих случаев заболевания – это следствие образования в женском яичнике нескольких клеточных генераций с мутированными и обычными аллеями дистрофина. При этом наиболее распространенным типом мутации (около 65%) являются значительные потери участков хромосомы.
Патология передается по аутосомно-рецессивному типу, со сцепкой с X-хромосомой (поражает мужские особи). Больше половины таких патологий возникают спонтанно, в связи с мутацией генов.
При генетическом обследовании большую роль играет определение у сестер пациента скрытых признаков заболевания. От такой носительницы мутированного гена может произойти передача патологии 50% её детей мужского пола, а 50% её дочек станут такими же носителями мутированного гена.
По мере того как заболевание прогрессирует, симптомы становятся все более выраженными, так как мышцы уже почти не способны обеспечивать нормальные движения. Мышцы рук постепенно слабеют, и ребенок с трудом может поднимать и удерживать предметы. Мышцы конечностей становятся ригидными, суставы теряют подвижность.
Очень часто деформируются локтевые, тазобедренные и коленные суставы. Мышцы, поддерживающие позвоночник, атрофируются, вследствие чего позвоночник искривляется. Ребенку становится все труднее ходить. У некоторых детей возникают проблемы с учебой. Обучение дается им с большим трудом, они не успевают по всем предметам.
Миопатия Дюшена — это наследственная болезнь, причём носителями поражённого гена являются женщины, которые сами никогда не болеют этим недугом. Наследуется ген по рецессивному типу, который связан с Х-хромосомой. При этом большинство выявленных случаев болезни – это мутации, которых раньше не было. Само заболевание является самым злокачественным из всех видов миопатий, к тому же недуг очень быстро прогрессирует, и остановить этот процесс невозможно.
Болезнь у ребёнка начинает проявляться не сразу после рождения, а только в возрасте от 1,5 до 5 лет. Первыми её признаками можно считать такие проявления, как:
- Неустойчивая походка.
- Неловкость в движении.
- Постоянные падения при ходьбе.
- Походка становится «утиной».
- Если ребёнку нужно подняться по лестнице, то он старается этого избегать.
- Трудности в подъёме из положении лёжа или сидя.
Ещё один важный признак этой болезни – это мнимая гипертрофия мышц. Кажется, что у ребёнка мышцы сильные и большие, но это мнение ошибочно. В реальности же идёт не развитие мышц, а их быстрое перерождение в жировую, и даже соединительную ткань.
Ещё один важный симптом – это обязательное поражение сердца, причиной которого является переизбыток в клетках сердца дистрофина.
По мере развития заболевания в суставах начинают появляться контрактуры, а к 10 – 12 годам ребёнок уже практически не может самостоятельно ходить, и ему потребуется инвалидное кресло. В 15 лет мальчик становится глубоким инвалидом.
Мышечная дистрофия у детей
Детство. Многие его вспоминают с улыбкой. Прятки, качели, велосипеды… Да сколько еще различных игр придумывает детвора. Но есть малыши, которые не могут себе позволить такой роскоши. Мышечная дистрофия у детей не дает такой возможности.
Практически все, за редким исключением, формы могут проявляться у деток своей симптоматикой: и злокачественная форма патологии по Дюшону (развивающаяся только у мальчиков), и доброкачественная мышечная дистрофия по Беккеру и другие. Особенно опасна патология, развивающаяся стремительно, агрессивно (форма по Дюшону). Причем для малыша опасна даже не столько сама симптоматика (атрофия практически всех групп мышц), как вторичные осложнения, которые и приводят к двадцати годам к смерти. Чаще всего летальный исход наступает вследствие респираторной инфекции или сердечной недостаточности. Но данная симптоматика становится более явной только тогда, когда малыш начинает делать первые шаги.
- Задержка в развитии: такие дети позже начинают сидеть и ходить.
- Медленное интеллектуальное развитие.
- Первыми поражаются мышцы позвоночника.
- Таким малышам трудно бегать и подниматься по лестнице.
- Походка вперевалочку.
- Деформация позвоночника.
- Ходьба на пальцах.
- Малышу тяжело держать свой вес, и он быстро утомляется.
- За счет жировой ткани увеличивается размер мышц.
- Поражение конечностей идет симметрично.
- Патологическое увеличение челюсти и промежутков между зубками.
- Приблизительно с 13 лет малыш перестает ходить совсем.
- Патология сердечной мышцы.